Величина щоденного дефіциту енергії передбачає частоту, але не тяжкість порушень менструального циклу, пов’язаних із фізичними вправами та обмеженням калорій
Лабораторія жіночого здоров’я та фізичних вправ та кафедра кінезіології, Університет штату Пенсильванія, Університетський парк, штат Пенсільванія; і
Адреса для запитів на передрук та іншої кореспонденції: Н. І. Вільямс, департамент кінезіології, лабораторія жіночого здоров’я та фізичних вправ, лабораторія Noll 108, Університет штату Пенсільванія, Університетський парк, штат Пенсільванія, 16802 (електронна пошта: [електронна пошта захищена]).
Лабораторія жіночого здоров’я та фізичних вправ та кафедра кінезіології Пенсильванського державного університету, Університетський парк, Пенсильванія; і
Лабораторія жіночого здоров’я та фізичних вправ та кафедра кінезіології Пенсильванського державного університету, Університетський парк, Пенсильванія; і
Лабораторія жіночого здоров’я та фізичних вправ та кафедра кінезіології, Університет штату Пенсильванія, Університетський парк, штат Пенсільванія; і
Медичний центр М. С. Герші, кафедра акушерства та гінекології, Медичний коледж Пенсильванського державного університету, Герші, штат Пенсільванія
Лабораторія жіночого здоров’я та фізичних вправ та кафедра кінезіології Пенсильванського державного університету, Університетський парк, Пенсильванія; і
Анотація
порушення менструального циклу у фізично активних жінок та спортсменок спостерігаються часто. Часто повідомляються порушення та відповідні показники поширеності включають дефекти лютеїнової фази (29%), ановуляцію (20%), олігоменорею (7%) та аменорею (37%) (12). Велика кількість доказів у різних видів ссавців продемонструвала причинно-наслідковий зв'язок між хронічним дефіцитом енергії та пригніченням репродуктивної функції, що включає центральне пригнічення пульсації гонадотропін-рилізинг-гормону (GnRH) (34). У людини тривалий енергетичний дефіцит може призвести до функціональної гіпоталамічної аменореї (FHA) і, отже, зменшити вплив естрогену, зменшивши вплив естрогену на кісткову, репродуктивну та серцево-судинну регуляції, що часто призводить до остеопенії (29, 34), стресових переломів (1, 3, 5), минуще безпліддя, дисліпідемія та порушення функції ендотелію (14, 15, 26). Проспективні дослідження підтверджують причинно-наслідкову роль низької енергетичної готовності на придушення репродуктивної функції, яка зазвичай спостерігається у фізично активних жінок та спортсменок (6, 20, 39).
Огляд експериментального дизайну.
У цьому дослідженні використано рандомізований перспективний дизайн, який використовував контрольоване годування та контрольовані лабораторні вправи протягом трьох менструальних циклів у молодих, нетренованих, передменопаузальних, еуменорейних жінок. Дослідження проводилось протягом 3 років, щорічні когорти набиралися восени навчального року і проводились до кінця весняного семестру. Контрольоване годування та фізичні вправи розпочалися після скринінгу та початкового періоду, причому кожен період тривав один менструальний цикл. Усі фази втручання були пов'язані з менструальними циклами випробовуваних, і кожна фаза дослідження складалася з одного менструального циклу (цикл втручання 1, цикл втручання 2, і цикл втручання 3). Період після дослідження протягом 1 тижня, коли дієта та фізичні вправи залишались контрольованими, дозволяв проводити вимірювання після втручання. Структура дослідження проілюстрована в таблиці 1. Групові завдання базувались на різному рівні енергетичного дефіциту, створеного за рахунок поєднання обмежень калорій та фізичних вправ, причому одна група залишалася в енергетичному балансі, а чотири групи мали різний ступінь дефіциту енергії. Були проведені неодноразові оцінки менструального стану, метаболічного стану та складу тіла.
Таблиця 1. Експериментальні процедури
RMR, швидкість метаболізму в спокої; CBC, загальний аналіз крові; V̇ o 2max, максимальна аеробна ємність. Примітка: тестування складу тіла середнього ступеня відбулося під час цикл втручання 2 для більшості предметів, але в деяких предметах це сталося протягом цикл втручання 3.
Предмети.
Включені критерії включення для дослідження 1) відсутність серйозних захворювань в анамнезі, 2) жодних поточних доказів невпорядкованого харчування чи розладу харчової поведінки в анамнезі немає, 3) вік 18–30 років, 4) вага 45–75 кг, 5) жир у тілі 15–35%, 6) ІМТ 18–25 кг/м 2, 7) номера для некурящих, 8) відсутність вживання ліків, які могли б змінити рівень метаболічного гормону, 9) відсутність значної втрати/набору ваги (± 2,3 кг) за останній рік, 10) 5,0 нг/мл) протягом базового циклу для підтвердження овуляції. Менструальні календарі використовували для документування менструальних кровотеч (і, отже, тривалості циклу) та виникнення судом або інших менструальних симптомів.
Якщо суб'єкти вважалися в доброму стані здоров'я і мали принаймні два послідовних овуляторних цикли, їх рандомізували в групи суб'єктів.
Групування предметів.
Менструальний статус.
Тривалість менструального циклу та менструальні симптоми були задокументовані протягом усього дослідження за допомогою менструальних календарів. Щоденні зразки сечі збирали протягом базового та цикли втручання 1–3 за раніше опублікованими методами (36). Експозиція естрогену та прогестерону, підтвердження овуляторного статусу, наявність або відсутність дефектів лютеїнової фази та тривалість фолікулярної та лютеїнової фаз визначали шляхом аналізу добових метаболітів естрону-1-глюкуроніду (E1G), прегнандіолу глюкуроніду (PdG) ) та середній цикл ЛГ після завершення дослідження з використанням раніше опублікованих методів (11). Характерні порушення менструального циклу включали дефекти лютеїнової фази, олігоменорейні цикли та ановуляторні цикли. Два типи дефектів лютеїнової фази, короткі лютеїнові фази (o 2 max визначали під час скринінгу, базову лінію, кожен цикл втручання та після дослідження. V̇ o 2 max визначали на основі додаткового тесту фізичних вправ на виснаженні бігової доріжки за допомогою модифікованого Протокол Астранда, що використовує непряму калориметрію (модель метаболічного кошика Sensormedics № 229; Sensormedics, Yorba Linda, CA) (28).
Забір крові.
Для всіх зразків крові суб'єкти голодували протягом ночі перед забором крові, що відбувалося між 0700 і 1000 в GCRC після лежання на спині протягом ≥15 хв. Кров давали згорнутися протягом 1 год перед центрифугуванням. Сироватку зберігали при -20 ° C до подальшого аналізу.
Біохімічні аналізи.
Статистика та аналіз даних.
Таблиця 2. Вихідні демографічні характеристики досліджуваних, класифікованих за групами
Значення виражаються як середні значення ± SE. EXCON, контроль здійснення; ЕД, дефіцит енергії (групи 1–3); ПА, фізичні навантаження.
a Дані з 3-денних журналів дієти.
Дотримання приписів дієти та фізичних вправ.
Призначена споживання калорій і фактичне споживання калорій варіювались
Таблиця 3. Параметри енергетичного балансу, усереднені за циклами втручання 1–3 для кожної групи
Фактична інтенсивність тренувань протягом усього втручання не відрізнялася серед груп і становила 76–79% від максимального пульсу (діапазон 73–89%) для всіх випробовуваних. V̇ o 2 max значно покращився (ефект часу P o 2 max = 37,9 ± 0,7 мл · кг −1 · хв -1 та пост-V̇ o 2 макс = 44,2 ± 1,6 мл · кг −1 · хв −1). Вага тіла з часом значно зменшилася (P 0,05), але T3 суттєво знизився у всіх групах, крім EXCON. Аналогічно, IGF-I не відрізнявся між групами на початковому рівні (EXCON 379,4 ± 30 мг/мл, ED1 346,8 ± 23 мг/мл, ED2 399,9 ± 30 мг/мл та ED3 366,0 ± 29 мг/мл), але значно знизився час у всіх групах, крім EXCON.
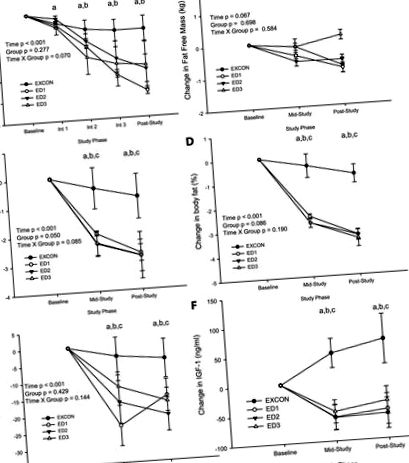
Рис. 1.Зміна маси тіла (кг; A), знежирена маса (кг; B), жирова маса (кг; C.), %тілесний жир (D), трийодтиронін (Т3; Е) та IGF-I (нг/мл; F) від базової лінії до цикл втручання 1 (Int 1), цикл втручання 2 (Int 2) та цикл втручання 3 (Int 3) (A) або базовий, середній та післястудійний (B-F) у всіх групах. A: вага тіла (кг), що здійснює контроль (EXCON), n = 8; дефіцит енергії (ЕД) 1, n = 6; ED2, n = 12; ED3, n = 8. B: маса без жиру (кг) EXCON, n = 6; ED1, n = 6; ED2, n = 11; ED3, n = 8. C.: жирова маса (кг) EXCON, n = 6; ED1, n = 6; ED2, n = 11; ED3, n = 8. D:% жиру EXCON, n = 6; ED1, n = 6; ED2, n = 11; ED3, n = 8. Е: T3 EXCON, n = 6; ED1, n = 5; ED2, n = 11; ED3, n = 8. F: IGF-I EXCON, n = 6; ED1, n = 5; ED2, n = 11; ED3, n = 8. Для A-Е, ANOVA з основними ефектами багаторазового вимірювання з тестуванням post hoc, використовуючи корекцію Бонферроні для виділення часового ефекту: ED1 проти базового рівня, P b ED2 проти базового рівня P c ED3 проти базового рівня, P a ED1, P b ED2, P c ED3, P
Вплив втручання на характеристики менструального циклу.
Жодної суттєвої зміни тривалості менструального циклу або тривалості фолікулярної фази не спостерігалося в жодній групі (табл. 4). Тривалість лютеїнової фази з часом суттєво зменшувалась у всіх групах (P
Таблиця 4. Вплив втручання на тривалість менструального циклу
Значення виражаються як середні значення ± SE.
Час, P b Час, P = 0,01 проти базового циклу; ANOVA з повторними заходами для кожної групи окремо.
Таблиця 5. Кількість та відповідний відсоток суб'єктів, що мають принаймні 1 з кожного типу менструальних розладів/загальна кількість суб'єктів у кожній групі для кожного циклу втручання
LPD, дефект лютеїнової фази. Примітка: підсумки втручання відображають число суб'єктів, які мали хоча б одне порушення менструального циклу протягом цикли втручання 1–3. Якщо у випробовуваних було більше одного порушення, їх підраховували лише один раз. У стовпці "Усього всіх груп" відображається "ні". суб'єктів, які мали принаймні одне порушення при розгляді всіх груп. Якщо у випробовуваних було більше одного порушення, їх підраховували лише один раз.
Рис.2.Частота кожного порушення менструального циклу, що спостерігається протягом втручання в кожній групі. Дані подаються як середні значення ± SE загальної суми порушень на групу. суттєво відрізняється від EXCON; b суттєво відрізняється від EXCON та ED1. Дані подаються як середні значення ± SE.
Рис.3.Середньодобовий енергетичний дефіцит (%), який спостерігався на всіх етапах дослідження (A) та сума всіх порушень менструального циклу протягом втручання для кожної групи (B). Дані подаються як середні значення ± SE. A: ED1 суттєво відрізняється від EXCON; b ED2 суттєво відрізняється від EXCON; c ED2 суттєво відрізняється від EXCON та ED1; d ED3 суттєво відрізняється від EXCON, ED1 та ED2. B: суттєво відрізняється від EXCON; b суттєво відрізняється від EXCON та ED1. Дані подаються як середні значення ± SE.
Коли всіх суб'єктів з усіх груп розглядали разом у поетапному багаторазовому лінійному регресійному аналізі для прогнозування частоти всіх менструальних порушень, спостерігалася залежність доза-реакція між частотою всіх типів порушень та величиною дефіциту енергії. Тобто середній відсоток дефіциту енергії був суттєвим предиктором частоти порушень менструального циклу (f = 10,1, β = −0,49, р 2 = 0,24, P = 0,003). Цікаво, що втрата ваги в кілограмах, втрата жиру в кілограмах та зміна RMR не були значущими предикторами частоти порушень менструального циклу, якщо включити їх у модель.
Це перше дослідження, яке продемонструвало залежність доза-реакція між величиною дефіциту енергії та частотою порушень менструального циклу, пов’язаних із фізичними вправами. Крім того, це дослідження демонструє два важливі клінічні висновки. 1) Коли молоді жінки відчувають еквівалент впливу трьох менструальних циклів енергетичного дефіциту в діапазоні від -8 до -42% від їх типових енергетичних потреб, найчастішою формою порушення менструального циклу, що виникає, є дефекти лютеїнової фази, що характеризуються або короткою ( Гранти Національних інститутів охорони здоров’я RO1-HD-39245-01 (NI Williams) та M01-RR-10732 та Департамент кінезіології, лабораторія жіночого здоров’я та фізичних вправ Пенсільського університету .
Авторам нічого розкривати.
N.I.W. концепція та дизайн дослідження; N.I.W. та H.J.L. проводили експерименти; N.I.W., H.J.L., B.R.H. та M.J.D.S. проаналізовані дані; N.I.W., R.S.L. та M.J.D.S. інтерпретовані результати експериментів; N.I.W. підготовлені фігури; N.I.W. складений рукопис; N.I.W., J.L.L., R.S.L. та M.J.D.S. відредагований та перероблений рукопис; N.I.W. затверджена остаточна версія рукопису.
ПОДЯКИ
Ми дякуємо Ен Каткарт, Тому Парротту, Брайану Фрай, Келлі Догерті, Мередіт Снук, Еріці Річардс та Джекі Гарднер за їх важливий внесок у це дослідження. Ми також цінуємо надзвичайну співпрацю досліджуваних та експертну допомогу співробітників GCRC.
- Як розрахувати базальний рівень метаболізму та щоденне споживання енергії GymBeam Blog
- Як рибоза покращує ваш щоденний енергетичний кінець
- Прибирання будинку Видалення поганої енергії з дому
- Як 7 людей, хворих на діабет, розгойдують свій A1c, харчуючись 7 різних способів; Діабет щодня
- Як спортсмени повинні відчувати дефіцит калорій; Їжте, щоб виконувати