Нові варіанти лікування ожиріння та цукрового діабету 2 типу (оглядовий огляд) ☆, ☆ ☆, ★
Роберт Р. Генрі
Центр метаболічних досліджень, система охорони здоров’я Сан-Дієго та Каліфорнійський університет Сан-Дієго, Сан-Дієго, Каліфорнія, США
Роберт Чілтон
b Університетська лікарня серцево-судинних захворювань та інтервенційної кардіології, Сан-Антоніо, Техас, США
В. Тимоті Гарві
c Відділ наук про харчування, Університет Алабами в Бірмінгемі та Медичний центр Бірмінгема, Бірмінгем, штат Алабама, США
Анотація
Помірне зниження ваги (> 5%), яке асоціюється із покращенням показників глікемії у пацієнтів з дисглікемією, також зменшує наявність інших супутніх захворювань, включаючи дисліпідемію та гіпертонію, що завершується зниженим ризиком серцево-судинних захворювань. Зміни способу життя - це рекомендований попередній підхід до схуднення, з початковою метою зниження ваги - 10% ваги тіла, що досягається протягом 6 місяців зі швидкістю 1–2 фунта на тиждень, обраною як відповідна мета для зменшення тяжкості ожиріння. пов'язані фактори ризику. Впровадження та підтримка змін у способі життя, пов’язаних із втратою ваги, може бути складним завданням для багатьох пацієнтів. Тому іноді можуть знадобитися додаткові втручання. Баріатрична хірургія також може бути високоефективним варіантом зниження ваги та зменшення супутньої захворюваності, однак хірургічне втручання несе значні ризики і все ще застосовується лише для окремих пацієнтів з діабетом 2 типу. Таким чином, увага звертається на використання препаратів для схуднення, включаючи 2 нещодавно затверджені сполуки: лоркасерин двічі на день та комбінацію фентерміну та топірамату пролонгованого вивільнення один раз на добу, які, як показано, є безпечною та ефективною терапією при лікуванні ожиріння у пацієнтів з діабетом 2 типу.
1. Вступ
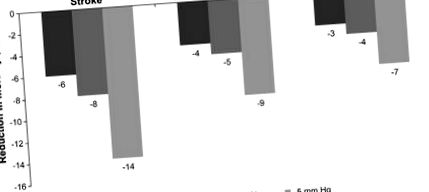
Зниження смертності за рахунок зниження систолічного артеріального тиску (SBP) (Chobanian et al., 2003; Whelton et al., 2002). Рисунок адаптовано за Уїлтоном та ін., 2002.
3.1. Зміни способу життя
Зміни способу життя, що включають модифікацію дієти, фізичну активність та поведінку, є початковими підходами до терапії для схуднення, рекомендованими Національним інститутом серця, легенів та крові (NHLBI) (Національний інститут серця, легенів та крові. Клінічні рекомендації щодо ідентифікації, 1998). Рекомендації NHLBI стверджують, що початкова втрата ваги на 10% маси тіла, досягнута за 6 місяців, зі швидкістю від 1 до 2 фунтів на тиждень, є відповідною метою для зменшення тяжкості факторів ризику ожиріння (Національне серце, легені, & Інститут крові. Клінічні вказівки щодо ідентифікації, 1998). ADA також рекомендує втрату ваги на 7% і більше для всіх осіб із надмірною вагою або ожирінням, які мають або ризикують розвинути СД2, посилаючись на зниження калорій, фізичну активність та модифікацію поведінки як на важливі елементи допомоги та підтримання втрати ваги (Американська діабетична асоціація, 2012).
У дослідженні Look AHEAD (Дія на користь здоров’я при діабеті) втрата ваги на 8,6% при інтенсивному втручанні у спосіб життя (таблиця 1) була пов’язана зі значним поліпшенням факторів ризику ССЗ у 5145 учасників із надмірною вагою/ожирінням з T2DM (таблиця 2) (див. AHEAD Research Group et al., 2007). Під час стратифікації цих пацієнтів за ступенем втрати ваги ті, хто досягли зниження ваги на 5% від a до вихідного рівня до 4 року (P =, 0032 проти PBO)
SBP знизився (P a 75-г пероральний тест на толерантність до глюкози (OGTT) проводили на початковому рівні, а потім кожні 6 місяців. Діагностика T2DM базувалася на одноразовому вимірі глюкози у цілій крові ≥ 10 ммоль/л.). перші 6 місяців дослідження, шляхом внесення змін до протоколу, пацієнтам із діабетичним ОГТТ повторно проводили ОГТТ протягом 4 тижнів. Повторний позитивний тест базувався на 2-годинній глюкозі цільної крові ≥10 ммоль/л, глюкозі цільної крові натще ≥6,7 ммоль/л, або 2 послідовних вимірювання глюкози в крові натще ≥6,7 ммоль/л.
Втрату ваги лише за рахунок зміни способу життя часто важко здійснити та підтримати (Barte et al., 2010; UKPDS Group, 1990), причому майже половина пацієнтів не змогли зберегти ≥75% своєї початкової втрати ваги протягом 52 тижнів (Wadden et al. ., 2010). Тому медичні втручання, такі як хірургічне втручання або фармакотерапія, можуть бути необхідним допоміжним засобом у деяких пацієнтів.
3.2. Баріатрична хірургія
Баріатричну хірургію рекомендується розглядати дорослим з індексом маси тіла (ІМТ)> 35 кг/м 2 та T2DM, особливо якщо T2DM або супутні супутні захворювання важко контролювати за допомогою способу життя та фармакологічної терапії (American Diabetes Association, 2012). Хірургічне втручання може бути високоефективним варіантом зменшення ваги та супутньої патології, забезпечуючи медично значущу втрату ваги, яка зберігається у більшості пацієнтів більше 5 років (Національний інститут серця, легенів та крові. Клінічні рекомендації з ідентифікації, 1998). Показано, що баріатрична хірургія покращує функцію β-клітин підшлункової залози (Hofsø et al., 2011) і може зменшити потребу в ліках у хворих із ожирінням з Т2ДМ і в деяких випадках призвести до ремісії Т2ДМ та гіпертонії (таблиці 1 та 2) 2) (Cunneen, 2008; Kadera et al., 2009).
3.3.1.1. Побічні ефекти
Під час дослідження XENDOS найпоширенішими побічними ефектами при застосуванні орлістату були шлунково-кишкові шляхи, включаючи сплетення з виділеннями, маслянисті плямистість та екстреність калу; вони мали легкий та помірний характер (Davidson et al., 1999; Torgerson et al., 2004). Значне зниження жиророзчинних вітамінів (A, D, E, K1) у групі орлістатів відбулося порівняно з плацебо (Torgerson et al., 2004); однак середній рівень кожного оціненого вітаміну знаходився в межах контрольного діапазону протягом 4-річного дослідження. Суб'єкти, які отримують орлістат, отримують вказівки приймати вітамінні добавки ≥2 години до або після вечірньої дози (XENICAL 2012).
3.3.2. Лоркасерин
У 2012 році FDA затвердила препарат для схуднення лоркасерин, селективний агоніст рецепторів серотоніну 2С, який діє центрально для сприяння зниженню ваги за рахунок зменшення споживання їжі та сприяння ситості (BELVIQ 2012). Точний механізм дії не відомий. Оскільки лоркасерин діє на серотонінергічні рецептори, існує потенціал розвитку серотонінового синдрому, який проявляється у вегетативних, когнітивних та соматичних симптомах, які можуть загрожувати життю. Як результат, слід дотримуватися граничної обережності, коли лоркасерин застосовується у поєднанні з іншими серотонінергічно діючими препаратами, включаючи, але не обмежуючись цим, селективні інгібітори зворотного захоплення серотоніну-норадреналіну, селективні інгібітори зворотного захоплення серотоніну, триптани та інгібітори моноаміноксидази (BELVIQ 2012).
Лоркасерин рекомендується вводити в дозі 10 мг перорально два рази на добу разом із втручанням у спосіб життя, включаючи дієту зі зниженою калорійністю та підвищену фізичну активність. Через 12 тижнів терапію слід оцінити, і якщо пацієнт не втратив ≥5% від базової маси тіла, терапію лоркасерином слід припинити (BELVIQ 2012).
3.3.2.1. Втрата ваги
3.3.2.3. Побічні ефекти
Під час випробувань BLOOM та BLOSSOM найпоширенішими побічними явищами були інфекції верхніх дихальних шляхів, головний біль, запаморочення, назофарингіт та нудота (Fidler et al., 2011; Smith et al., 2010). Частота визначеної FDA вальвулопатії через 1 рік була еквівалентною у всіх групах: 2,7% у групі лоркасерину в дозі 10 мг проти 2,3% у групі плацебо у дослідженні BLOOM та 2,0%, 1,4% та 2,0% у лоркасерині 10 mg BID, лоркасерин 10 мг QD та групи плацебо відповідно у дослідженні BLOSSOM (Fidler et al., 2011; Smith et al., 2010). Як і при випробуваннях BLOOM та BLOSSOM, найпоширенішими побічними явищами, про які повідомляли суб’єкти з T2DM у дослідженні BLOOM-DM, були головний біль, біль у спині, назофарингіт та нудота (O’Neil et al., 2012). На 52-му тижні у дослідженні BLOOM-DM 2,9% та 2,5% лоркасерину 10 мг два рази на добу та лоркасерину 10 мг QD T2DM відповідно повідомляли про нову вальвулопатію, але показник у пацієнтів, які отримували плацебо з Т2ДМ, знизився до 0,5%; ці зміни не були суттєвими (O’Neil et al., 2012). Крім того, гіпоглікемія, про яку повідомляли пацієнти, спостерігалася у 29,3% суб'єктів, які отримували лоркасерин 10 мг два рази на добу, і 21,0% суб'єктів, які отримували плацебо (BELVIQ 2012), причому симптоматична гіпоглікемія спостерігалася у 7,4% пацієнтів з Т2ДМ, які отримували лоркасерин 10 мг два рази на день, 10,5% отримували лоркасерин 10 мг на добу і 6,3% отримували плацебо; обидва вони були частішими у пацієнтів, які отримували сульфонілсечовини (O’Neil et al., 2012).
3.3.3. Фентермін та топірамат з пролонгованим вивільненням
Запропоновано алгоритм лікування, щоб максимізувати користь та ризик для пацієнта. Лікування слід починати з PHEN 3,75 мг/TPM ER 23 мг (3,75/23) QD протягом 2 тижнів (14 днів), а потім збільшувати до PHEN 7,5 mg/TPM ER 46 mg (7,5/46) QD протягом 12 тижнів (QSYMIA 2012) . Втрату ваги слід оцінювати через 12 тижнів у дозі 7,5/46, і якщо пацієнт не втратив ≥3% маси тіла, лікування слід припинити або дозу збільшити до PHEN 15 мг/TPM ER 92 мг (15/92 ) у двоступеневому процесі, збільшуючи до PHEN 11,25 мг/TPM ER 69 мг QD протягом 2 тижнів з подальшим 15/92 QD протягом 12 тижнів. Якщо після додаткових 12 тижнів лікування 15/92 пацієнт не втратив ≥5% від базової маси тіла, лікування слід припинити відповідно до вказівок.
Ефективність та безпеку PHEN/TPM ER оцінювали у двох 1-річних рандомізованих подвійних сліпих плацебо-контрольованих дослідженнях фази 3. Дослідження EQUIP оцінило 1267 дорослих із ожирінням (ІМТ ≥35 кг/м 2), рандомізованих на плацебо, 3,75/23 або 15/92 (Allison et al., 2012). У дослідженні CONQUER було оцінено 2487 дорослих із надмірною вагою та ожирінням (ІМТ ≥27 кг/м 2 та ≤45 кг/м 2) із ≥2 супутніми захворюваннями, пов’язаними з вагою, включаючи T2DM та серцево-судинні захворювання (Gadde et al., 2011). Суб'єкти були рандомізовані на плацебо, 7,5/46 або 15/92. Після перших 56 тижнів лікування в CONQUER 676 суб'єктів на підмножині сайтів продовжили розширене дослідження SEQUEL, яке оцінювало суб'єктів протягом додаткових 52 тижнів, зберігаючи їх початкову сліпу рандомізацію (Garvey et al., 2012). Всім випробовуваним вдалося отримати стандартну допомогу щодо відповідних супутніх захворювань, включаючи T2DM, і вони отримували дієтичні та життєві консультації на основі програми LEARN (Brownell, 2000).
3.3.3.1. Втрата ваги
У дослідженні EQUIP використання PHEN/TPM ER призвело до значної втрати ваги протягом 56 тижнів у порівнянні з плацебо, і більше пацієнтів досягли втрати ваги на ≥5% за 1 рік, ніж ті, хто отримував плацебо (P Таблиця 1) (Allison et al., 2012). Через 1 рік у дослідженні CONQUER середній відсоток втрати ваги LS у загальній популяції був значно більшим, ніж при застосуванні плацебо (P Таблиця 1) (Gadde et al., 2011), і підтримувався протягом 2 років у дослідженні SEQUEL (P Таблиця 1; Мал. 2C) (Garvey et al., 2012). У дослідженні CONQUER більше суб'єктів, які отримували PHEN/TPM ER, досягли втрати ваги на ≥5% за 1 рік, ніж ті, хто отримував плацебо (P Таблиця 1) (Gadde et al., 2011), і це також зберігалося протягом 2 років у випробування SEQUEL (P Таблиця 1) (Garvey et al., 2012). Подібним чином, у тих суб'єктів, у яких на початковому рівні був T2DM, через 1 рік лікування спостерігали значну середню частку втрати ваги середнього рівня (P Fig. 2D) (Gadde et al., 2011; Garvey, Peterson, & Troupin, 2010). Спільний аналіз результатів клінічних випробувань показав, що 83,5% пацієнтів, які закінчили 12 тижнів лікування 7,5/46, були респондентами (≥3% втрати ваги через 12 тижнів), як визначено на етикетці (Dvorak, Peterson, & Day, 2012; QSYMIA 2012).
3.3.3.2. Кардіометаболічні параметри
Як і в загальній популяції, у досліджуваних CONQUER (табл. 2) у досліджуваних CONQUER (табл. 2) суб’єкти з T2DM на вихідному рівні, які отримували PHEN/TPM ER, мали більші показники покращення показників глікемії на 1 рік (табл. 2). Ці поліпшення глікемічних показників були більшими при PHEN/TPM ER, ніж при плацебо, і менша кількість цих активно керованих суб'єктів, які отримували PHEN/TPM ER, потребувала збільшення супутніх протидіабетичних препаратів (Gadde et al., 2011): 12,1% пацієнтів з T2DM у групі плацебо потрібно чисте збільшення антидіабетичних препаратів порівняно з лише 1,5% та 0,6% пацієнтів у групах 7,5/46 та 15/92 відповідно (Garvey et al., 2010).
3.3.3.3. Побічні ефекти
У дослідженні EQUIP найпоширенішими побічними явищами були парестезія, сухість у роті, запор, головний біль, дисгевзія та безсоння (Allison et al., 2012); у дослідженні CONQUER сухість у роті, парестезія, запор, безсоння, запаморочення та дисгевзія. Подібним чином типи побічних явищ, що виникають між 1 і 2 роками у дослідженні SEQUEL, були подібними до тих, про які повідомлялось у загальній вибірці CONQUER від початкового рівня до 1 року, хоча частота окремих побічних ефектів, що виникали під час лікування, була помітно нижчою на другий рік (56–108 тижнів) (Garvey et al., 2012). У EQUIP та CONQUER спостерігалось невелике збільшення середньої частоти серцевих скорочень: EQUIP, -0,2, -0,3 та 1,2 уд./Хв при плацебо, 3,75/23 та 15/92, відповідно (Allison et al., 2012); CONQUER, -0,1, 0,1 та 1,7 ударів на хвилину з плацебо, 7,5/46 та 15/92, відповідно (Gadde et al., 2011; Garvey et al., 2012). Однак середнє АТ знизилось при лікуванні PHEN/TPM ER порівняно з плацебо, і не повідомлялося про небажані явища, пов'язані зі зміною частоти серцевих скорочень (Allison et al., 2012; Gadde et al., 2011; Garvey et al., 2012 ).
3.4. Досліджувані фармакотерапії для схуднення
3.4.1. Налтрексон пролонгованого вивільнення та бупропіон пролонгованого вивільнення
Додатковою терапією, яка досліджується для лікування ожиріння, є комбінація налтрексону із затримкою вивільнення (SR) та бупропіону SR. Програма досліджень ожиріння Contrave (COR) складалася з чотирьох 1-річних досліджень 3 фази пацієнтів із надмірною вагою/ожирінням: COR-I (Greenway et al., 2010), COR-II (Rubino et al., 2010) та COR -Модифікація поведінки (COR-BMOD) (Wadden et al., 2011), яка виключала учасників з T2DM; та COR-Diabetes Mellitus (CORDM) (Hollander et al., 2010), який включав учасників з T2DM (Makowski, Gwinn, & Hurren, 2011). Учасники COR-I, COR-II та COR-DM отримували консультації щодо способу життя, включаючи зменшення споживання енергії на 500 ккал/день та збільшення фізичної активності, на початковому етапі та кожні 12 тижнів (Greenway et al., 2010; US Food & Drug Адміністрація, 2012). Крім того, учасники випробування COR-BMOD відвідували 90-хвилинні мультидисциплінарні групові відвідування щотижня протягом 16 тижнів і щомісяця, після чого їм призначали дієти від 1200 до 2000 ккал/день та спонукали займатися фізичними навантаженнями протягом 180 хв на тиждень протягом перших 6 місяців, збільшуючись до 360 хв на тиждень після цього (Wadden et al., 2011).
У кожному з цих випробувань налтрексон SR/бупропіон SR спричиняв більшу втрату ваги та покращення кардіометаболічних показників у порівнянні з плацебо (таблиця 1) (Greenway et al., 2010; Makowski et al., 2011; US Food and Drug Administration, 2012; Wadden et al., 2011). У дослідженні CORDM серед пацієнтів з T2DM, які застосовували перорально або не застосовували протидіабетичні препарати, було виявлено, що налтрексон SR/бупропіон SR викликає значну втрату ваги та покращення рівня HbA1c, а також покращення окружності талії, тригліцеридів та холестерину ЛПВЩ (табл. 2). (Hollander et al., 2010; Makowski et al., 2011; US Food and Drug Administration, 2012). У всіх випробуваннях, після 56 тижнів лікування, групи плацебо зазнали більшого зниження рівня SBP та DBP, ніж групи налтрексону SR/бупропіон SR (Makowski et al., 2011; US Food and Drug Administration, 2012). У дослідженнях фази 3 найпоширенішими побічними явищами були нудота, запор, головний біль, блювота та запаморочення. Крім того, через 56 тижнів частота серцевих скорочень збільшувалася в середньому на 0,3 ударів на хвилину при застосуванні налтрексону SR/бупропіон SR проти -0,98 ударів на хвилину при плацебо (Makowski et al., 2011; US Food and Drug Administration, 2012).
У січні 2011 року FDA видала Orexigen, виробника налтрексону SR/бупропіону SR, повний лист-відповідь, в якому було запропоновано дослідження серцево-судинних результатів (CVOT; The Light Study). Orexigen ініціював зарахування до CVOT у травні 2012 року. Орієнтовна дата завершення CVOT - липень 2017 року. Дата завершення буде залежати від часу, необхідного для накопичення достатньої кількості подій для статистичної оцінки коефіцієнтів ризику на основі проміжного аналізу. Первинним показником результату буде час від рандомізації періоду лікування до першого підтвердженого виникнення серйозних несприятливих серцево-судинних подій (MACE), з вторинними кінцевими точками, включаючи час від рандомізації періоду лікування до першої підтвердженої серцево-судинної смерті, інфаркту міокарда (летальний/нефатальний ), інсульт (летальний/нефатальний) та нестабільна нестабільна стенокардія, що вимагає госпіталізації (Серцево-судинні результати, 2012). Суб'єкти включатимуть надмірну вагу та ожиріння (ІМТ ≥27 та ≤50 кг/м 2) дорослих ≥45 років, які мають високий ризик зазнати цих подій через T2DM та/або інші фактори серцево-судинного ризику; учасники будуть рандомізовані на плацебо або налтрексон SR 32 мг/бупроприон SR 360 мг/день.
3.4.2. Ліраглутид
4. Висновок
Оскільки показники ожиріння та СД2 продовжують зростати, потреба в ефективних стратегіях схуднення стає більш актуальною. Хоча втручання у спосіб життя та баріатрична хірургія зменшують масу тіла та покращують фактори ризику, пов’язані з T2DM та ССЗ, лише втручання у спосіб життя важко підтримувати, а баріатрична хірургія, доступна обмеженому колу пацієнтів, може бути пов’язана з більшою ризики. На даний момент доступний орлістат демонструє лише помірну втрату ваги, а прихильність обмежується переносимістю. Лоркасерин та PHEN/TPM ER були нещодавно схвалені FDA, і клінічні випробування продемонстрували як значну, тривалу втрату ваги в порівнянні з плацебо, так і поліпшення глікемічних показників та факторів ризику кардіометаболізму у пацієнтів із надмірною вагою/ожирінням із Т2ДМ та без нього. Як лоркасерин, так і PHEN/TPM ER добре переносились у клінічних дослідженнях, і вони будуть дотримуватися для довготривалої безпеки. Ці результати дозволяють припустити, що лоркасерин або PHEN/TPM ER, використовуючи разом із модифікацією способу життя, можуть представляти безпечну та ефективну терапію для лікування ожиріння у пацієнтів з T2DM.
Подяка
Ми хотіли б подякувати та подякувати The Lockwood Group за редакційну допомогу (фінансування було надано VIVUS, Inc.) та внутрішнім співробітникам VIVUS, Inc.
Виноски
☆ Д-р Генрі працював радником VIVUS, Inc. Д-р Гарві працював радником та слідчим VIVUS, Inc., а також є акціонером VIVUS, Inc. Д-р Чілтон є радником і доповідачем VIVUS, Inc.
☆ ☆ Підтримка: немає.
★ Фінансування: VIVUS, Inc., для допомоги в рукописах.
- Засоби природного ожиріння - рослинні; Варіанти лікування органічного ожиріння Природні
- Статеві гормони, ожиріння та цукровий діабет 2 типу є тут
- Цукрові підсолоджені напої, ожиріння, цукровий діабет 2 типу та ризик серцево-судинних захворювань
- Потенційний захист від діабету 2 типу при ожирінні завдяки нижчій експресії та покращенню CD36
- Поліморфізм генів SREBF-1 пов'язаний із ожирінням та діабетом 2 типу у французьких людей із ожирінням та