Не підозрювана метаболічна роль передсердних натрійуретичних пептидів
З IFR31-Інституту Луїса Бугнарда; Hôpital Rangueil, Institut National de la Santé et de la Recherche Médicale (Inserm), Inserm U586; відділ дослідження ожиріння; ВР 84 225; 31432 Тулуза седекс 4; та Університет Поля Сабатьє, 31052 Тулуза, седекс 4, Франція.
З IFR31-Інституту Луїса Бугнарда; Hôpital Rangueil, Institut National de la Santé et de la Recherche Médicale (Inserm), Inserm U586; відділ дослідження ожиріння; ВР 84 225; 31432 Тулуза седекс 4; та Університет Поля Сабатьє, 31052 Тулуза, седекс 4, Франція.
З IFR31-Інституту Луїса Бугнарда; Hôpital Rangueil, Institut National de la Santé et de la Recherche Médicale (Inserm), Inserm U586; відділ дослідження ожиріння; ВР 84 225; 31432 Тулуза седекс 4; та Університет Поля Сабатьє, 31052 Тулуза, седекс 4, Франція.
З IFR31-Інституту Луїса Бугнарда; Hôpital Rangueil, Institut National de la Santé et de la Recherche Médicale (Inserm), Inserm U586; відділ дослідження ожиріння; BP 84 225; 31432 Тулуза седекс 4; та Університет Поля Сабатьє, 31052 Тулуза, седекс 4, Франція.
З IFR31-Інституту Луїса Бугнарда; Hôpital Rangueil, Institut National de la Santé et de la Recherche Médicale (Inserm), Inserm U586; відділ дослідження ожиріння; ВР 84 225; 31432 Тулуза седекс 4; та Університет Поля Сабатьє, 31052 Тулуза, седекс 4, Франція.
З IFR31-Інституту Луїса Бугнарда; Hôpital Rangueil, Institut National de la Santé et de la Recherche Médicale (Inserm), Inserm U586; відділ дослідження ожиріння; ВР 84 225; 31432 Тулуза седекс 4; та Університет Поля Сабатьє, 31052 Тулуза, седекс 4, Франція.
Ви переглядаєте останню версію цієї статті. Попередні версії:
Анотація
Натрійуретичні пептиди (НП) є новими факторами, які можуть відкрити перспективні шляхи дослідження для пояснення контролю мобілізації ліпідів у фізіологічних та патологічних станах. Метаболічний вплив зміненого виробництва та циркуляції НП ще належить встановити. Потенційний вплив НП на розвиток розладів ліпідів, серцево-судинних подій, пов’язаних з ожирінням, та серцевої кахексії буде розглянуто в цьому огляді.
Ожиріння, НЕФА та патогенез цукрового діабету 2 типу
Структура розподілу жиру також є важливою змінною для метаболізму NEFA у цілому тілі та чутливості до інсуліну. Особи з накопиченням жиру у верхній частині тіла та вісцеральним жиром мають вищий ризик розвитку гіперінсулінемії, резистентності до інсуліну, дисліпідемії та діабету 2 типу. 20,21 Існує гіпотеза, що вісцеральний АТ-ліполіз вивільняє надлишки NEFA у ворітну вену, піддаючи печінку вищим концентраціям NEFA. 22 Внесок ліполізу вісцеральної жирової тканини у доставку печінки NEFA зростає із збільшенням вісцерального жиру у людей, і цей ефект більший у жінок, ніж у чоловіків. 23 Однак це становить дуже малий відсоток від загальної кількості НЕФА, доставлених до скелетних м'язів. 24 Враховуючи основну патогенну роль, що приписується порушенням регуляції NEFA, коротко будуть розглянуті механізми, що впливають на вивільнення NEFA жировими клітинами, та основні шляхи, що контролюють ліполітичну систему.
Ліполітичні шляхи та регулювання мобілізації ліпідів у людей
Катехоламіни та адренергічні рецептори жирових клітин
Адренергічний контроль ліполізу жирових клітин людини є складним через неоднорідність розподілу α2-/β1/2-AR у різних жирових відкладах. 21 У ряді досліджень in vitro чітко встановлено, що репертуар та рівень експресії адренергічних рецепторів адипоцитів людини значною мірою відрізняються залежно від анатомічного розташування та масштабів депо АТ, розміру адипоцитів, статі та віку досліджуваних. та генетичні детермінанти. Більше того, ліполітична стійкість до катехоламінів була продемонстрована в підшкірній АТ людини - головному жировому депо у людей із ожирінням. І навпаки, жирові клітини з вісцеральних відкладень демонструють найвищу β-адренергічну реакцію. Повідомлялося про придушений індукований адреналіном ліполіз у АТ пацієнтів із ожирінням. Відмінності в ліполітичній реакції на катехоламіни у людей із ожирінням порівняно з худими пацієнтами пов'язані з варіаціями експресії HSL та функціональним балансом між β- та α2-AR. Інші порушення в каналах передачі сигналу катехоламіну також можуть пояснити ліполітичні дефекти (див. Огляди 39,40).
Інсулін: основний антиліполітичний засіб
Інсулін відіграє важливу роль у контролі викидів NEFA. Інсулін є головним регулятором ліполізу. Він інгібує ліполіз та витік NEFA та стимулює засвоєння глюкози жировими клітинами та накопиченням жиру (тобто збільшує швидкість ресинтезу TAG з NEFA; ефект реестерифікації). Надходження НЕФА з АТ до інших тканин швидко та сильно пригнічується підвищенням плазмової концентрації інсуліну. Окреслено клітинні механізми, що беруть участь у пригніченні ліполізу інсуліном. 41,42 Інсулінозалежне інгібування ліполізу діє за допомогою стимуляції циклічним нуклеотидом фосфодіестераза-3B (PDE-3B), що сприяє гідролізу цАМФ, що призводить до зниження рівня внутрішньоклітинного цАМФ та інгібування ліполізу (рис. 1).
У ситуації після їжі або при внутрішньовенному введенні інсуліну за допомогою техніки еуглікемічного гіперінсулінемічного затиску ліполіз швидко та разюче пригнічується. Зниження рівня інсуліну в плазмі крові під час голодування, фізичних вправ або навіть після гострого введення соматостатину призводить до різкого збільшення швидкості ліполітики. Доведено, що низка факторів циркуляції крові (таких як TNF-α, ІЛ, сам інсулін, НЕФА та продукти глікування) впливає на дію інсуліну на рівні клітин-мішеней і може призвести до гіперглікемії та діабету 2 типу, коли їх дія змінюється. 43
Здається обґрунтованим припустити, що добре відомі метаболічні порушення, пов’язані з ожирінням верхньої частини тіла, можуть бути пов’язані з регіональними варіаціями регуляції ліполізу та вироблення НЕФА інсуліном. Зрозуміло, що помірні зміни рівня інсуліну натще або чутливості до інсуліну змінюють ліполіз жирових клітин та концентрацію NEFA в плазмі натще. Вражаючі відмінності, пов'язані з жировим депо, модульовані ожирінням, були виявлені в реакції жирових клітин на інсулін. Індуковане придушення ліполізу та активація реестерифікації NEFA притупляються у сальнику порівняно з клітинами підшкірної жирової клітковини. 44 Виявлено різні функціональні відмінності на рівні рецепторів інсуліну та на рівні післярецепторів сигнального каскаду інсуліну. 45 Інші партнери сигнального каскаду інсуліну, такі як PDE-3B та білково-тирозинфосфатази (PTPase), які беруть участь у дефосфорилюванні інсулінових рецепторів, також можуть сприяти модуляції дії інсуліну. Ендогенна активність PTPase, включаючи PTPase-1B, збільшується в жировій тканині сальникової залози і може сприяти відносній резистентності до інсуліну цього жирового депо. 46
Повідомлялося про збільшення вихідного системного потоку NEFA у жінок із ожирінням у верхній частині тіла. Вони частково пояснюються зниженою чутливістю до антиліполітичного ефекту інсуліну, незалежно від розміру жирових клітин, та збільшенням ліполітичних показників, пов’язаних із гіпертрофією клітин підшкірної жирової клітини. 47 Підшкірні черевні адипоцити стійкіші до антиліполітичного ефекту інсуліну, ніж сідничні адипоцити, незалежно від розміру клітин. 48 Результати in vivo підтвердили регіональну неоднорідність вивільнення NEFA, регульованого інсуліном, in vivo. Вісцеральна жирова тканина більш стійка до антиліполітичних ефектів інсуліну, ніж жир на ногах і непланхронному тілі. 49 Тим не менше, вісцеральний жир може бути маркером надлишкової кількості НЕФА після їжі, але не джерелом надлишкового ожиріння, оскільки збільшення викидів НЕФА після їжі, що спостерігається у жінок із ожирінням у верхній частині тіла та діабетиків типу 2, походить від непланхнічного жиру верхньої частини тіла, а не вісцерального жиру. 50
Натрійуретичні пептиди сприяють контролю ліполізу та мобілізації ліпідів у людей
Натрійуретичні пептиди
Натрійуретичні рецептори пептидів
NPR-A також були виявлені в жирових клітинах щурів. 78,79 Повідомлялося про слабкий приріст цГМФ, стимульований ANP, у жирових клітинах щурів. 80 Жирова тканина людини експресує передавальну РНК NPR-A та NPR-C. 81 Жодних біологічних реакцій у жирових клітинах людини не досліджували, коли були розпочаті наші перші дослідження. Функція рецептора NPR-C ніколи не досліджувалась у жирових клітинах.
Ліполітичний ефект натрійуретичних пептидів
Оригінальною знахідкою, яка стала поштовхом для подальших досліджень метаболічної ролі НП, було відкриття ліполітичної дії НП в ізольованих від людини жирових клітинах. НП мають сильний ліполітичний ефект, подібний до ефектів, викликаних агоністом β-AR, ізопротеренолом. Відносний порядок ліполітичної потужності пептидів (ANP> BNP≫CNP) припускав наявність рецептора NPR-A у жирових клітинах людини. Цей момент був підтверджений дослідженнями зв'язування, проведеними на мембранах жирових клітин людини з використанням [125 I] ANP як радіоліганда та різних конкурентів пептидів. 3
Важливо відзначити, що ліполітичний ефект НП повністю незалежний від основного антиліполітичного гормону - інсуліну. Інсулін добре відомий своїми антиліполітичними ефектами в жирових клітинах людини, що призводять до інгібування агоніста β-AR- (тобто ізопротеренолу) та індукованого катехоламінами ліполізу. Лікування інсуліном жирових клітин людини не впливає на ліполітичну відповідь, спричинену ANP. 3,82,87 Оскільки антиліполітичні ефекти інсуліну опосередковані зниженням внутрішньоклітинного рівня цАМФ, ініційованим активацією PDE-3B, зрозуміло, чому цей гормон не втручається в залежність від цГМФ ефектів НП. Заслуговує на увагу розмежування механізмів, що беруть участь у регулюванні дії НП. Хронічна стимуляція НП та патологічні стани, пов’язані з перевиробництвом НП, можуть обмежити реакцію жирових клітин шляхом десенсибілізації активності NPR-A. Гомологічна десенсибілізація ANP-залежного шляху після попереднього впливу на жирові клітини ANP була показана в ізольованих жирових клітинах in vitro. 87
Виникнення NP-індукованого ліполізу характерне для жирових клітин приматів. НП не стимулюють ліполіз в жирових клітинах інших видів, включаючи щурів, мишей, кроликів та собак. ANP збільшив базальну продукцію цГМФ у 300 разів у жирових клітинах людини, тоді як в адипоцитах щурів він стимулювався лише в 3 рази. Одне з основних пояснень таких вражаючих видів, пов'язаних з різницею у реакції жирових клітин на НП, полягає в тому, що адипоцити від видів, що не реагують на НП, експресують головним чином кліренс плазматичного кліренсу NPR-C та дуже низьку експресію біологічно активного NPR-A. Стимуляція невеликої популяції NPR-A на цих клітинах недостатня для збільшення приросту рівня цГМФ, необхідного для досягнення заданого значення для активації HSL. 88 Привертає увагу той факт, що цим новим ліполітичним шляхом мають лише примати. Однак відсутність моделей на тваринах не сприятиме подальшим дослідженням ролі та регулювання цієї системи.
Індукція мобілізації ліпідів місцевим або системним введенням АНП
Ліполітична дія, продемонстрована в ізольованих клітинах підшкірно-жирових клітин людини in vitro, була підтверджена in vivo при застосуванні ANP у мікродіалізному зонді, імплантованому в підшкірну черевну АТ людини (SCAAT). Мікродіаліз in situ пропонує кілька можливостей для клінічного дослідження судинних та метаболічних ефектів, ініційованих у підшкірній АТ місцевим або системним введенням препаратів або фізичними вправами. 89 Інфузія ANP у зонді для мікродіалізу підвищила позаклітинну концентрацію гліцерину в АТ та судинорозширила судини, що дренують жировий осад. 3 Обидві події сприяють скоординованому посиленню мобілізації ліпідів у SCAAT.
Внесок АНП у фізіологічний контроль мобілізації ліпідів у людей
Малюнок 2. Порівняння середніх змін концентрацій позаклітинного гліцерину в підшкірній жировій клітині черевної порожнини під час двох послідовних навантажень, виконаних при 35% (вправа 1) та 60% (вправа 2) V o max та під час відновлення. A, Вплив локальної блокади β-адренергічних рецепторів: Контрольний зонд для мікродіалізу перфузували буфером Кребса-Рінгера. Для вивчення місцевої блокади β-адренергічних рецепторів зонд для мікродіалізу доповнювали пропранололом (100 мкмоль/л). Пропранолол частково блокував збільшення ЕГК, спричинене фізичними вправами. β-адренергічна реакція жирових клітин була повністю заблокована. 95 B, Вплив пероральної блокади β-адренергічних рецепторів за допомогою тертатололу: Контрольний (плацебо) зонд для мікродіалізу перфузували буфером Кребса-Рінгера. Тертатолол (5 мг) вводили за 1 годину до тренування. Лікування тертатололом не впливає на збільшення EGC, спричинене фізичними вправами. Було підтверджено, що β-адренергічна реакція адипоцитів була повністю заблокована. 95
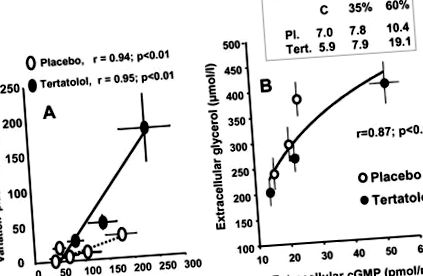
Малюнок 3. Порівняння середніх змін рівня АНП та цГМФ у плазмі крові, а також позаклітинного гліцерину (ЕГК) та концентрації цГМФ під час двох послідовних вправ, виконаних при 35% (вправа 1) та 60% (вправа 2) V o max у плацебо та тертатололі (антагоніст β-адренергічних рецепторів), які отримували лікування. 95 A, Кореляція між концентраціями АНП у плазмі крові та збільшенням концентрації позаклітинного гліцерину в зондах, перфузованих пропранололом у пацієнтів, які отримували плацебо та терталолол. Значення ANP та EGC визначали на 10-й та 20-й хвилинах кожного вправи. B, Кореляція між EGC та позаклітинними концентраціями cGMP. Концентрацію цГМФ, ЕГК та позаклітинного цГМФ визначали у спокої та під час кожного вправи.
Фізіологічні питання та майбутні тенденції
Перш ніж додавати новий ліполітичний засіб до списку перевірених ліпідмобілізуючих гормонів, необхідно визначити, чи здатна циркулююча або місцева (тобто на рівні адипоцитів) концентрація ліполітичного агента ініціювати мобілізацію ліпідів in vivo під час ліпідного мобілізуючий виклик. Результати ANP відповідають цьому правилу, хоча відсутність відповідного антагоніста NPR-A обмежує тлумачення. Дослідження ролі АНП за допомогою мікродіалізу проводили в SCAAT з практичних причин, пов'язаних із використанням методики мікродіалізу. Дія ANP на інші жирові відкладення має бути розширено найближчим часом, щоб перевірити, чи відрізняється чутливість жирових клітин до ANP/BNP залежно від анатомічного розташування жирових відкладень, як повідомляється для інших регуляторних шляхів. 21
Малюнок 4. Функціональні домени ANP-залежної рецепторної системи в жировій клітині людини. KHD вказує на регуляторний домен внутрішньоклітинної кінази-гомології; GC, каталітичний домен гуанілілциклази. Неприлізин (нейтральна ендопептидаза 24.11, CD10, NEP), який бере участь у деградації натрійуретичного пептиду, був ідентифікований в мембрані жирових клітин людини (C.M., M.B., M.L., неопубліковані результати, 2005).
Епідеміологічне дослідження, проведене у когорті нащадків Фрамінгемського дослідження серця, показало, що рівень ожиріння ANP та BNP у пацієнтів із ожирінням знижується. 105 Крім того, знижений рівень BNP спостерігається у людей із ожирінням із серцевою недостатністю. 106 Виникає змінений розподіл розподілу NPR-A/-C жирових клітин та зміна реакції на NP у людей, що страждають ожирінням. 107,108 Ці епідеміологічні дослідження повинні супроводжуватися функціональними дослідженнями, щоб окреслити механізми, що ведуть до змінених шляхів розвитку НП.
Патологічні питання та майбутні тенденції
Лікування антагоністом β-AR
Цукровий діабет 2 типу
Більшість пацієнтів з діабетом 2 типу мають надлишкову вагу або ожиріння. 113 Вони відчувають підвищення протягом дня концентрації NEFA у плазмі крові, яке призводить до нормального придушення їжею або навантаженням глюкози. 114 Оскільки підвищений циркулюючий НЕФА може спричинити/посилити резистентність до інсуліну в м’язах та печінці 16 та може збільшити ризик раптової смерті 19, важливо знати, чи працюють НП, крім інсулінорезистентності, як партнери при розладах, пов’язаних із метаболічним синдромом . Існують суперечки щодо рівня ANP/BNP у плазмі крові у хворих на цукровий діабет. 105
Застійна серцева недостатність та серцева кахексія
Гомологічна десенсибілізація залежних від ANP ефектів на ліполіз та мобілізацію ліпідів відбувається послідовно до гострого впливу ANP. 87 Враховуючи надмірне виділення NP, яке спостерігається при застійній серцевій недостатності, організм може адаптуватися до підвищеного рівня ендогенного BNP через зниження регуляції сигнальних шляхів NP в жировій тканині. Більше того, не можна виключати регуляцію очисних шляхів (тобто, збільшення експресії NPR-C кліренсу або посилену активність NEP).
Фармакологічні методи лікування
Ліки, які впливають на натрійуретичну пептидергічну систему (тобто агоністи NPR-A та інгібітори NEP 24.11), можуть спричинити метаболічні зміни. BNP (несіритид) зараз схвалений для лікування гострої серцевої недостатності, оскільки має сприятливий вплив на центральну гемодинаміку та виведення Na + з сечею. 112 120–122 Порівняно з ANP, BNP, здається, менш сприйнятливий до деградації за допомогою NEP 24.11 і може бути більш потужним натрійуретичним агентом, ніж ANP. 65 Буде важливо перевірити, чи сприяє інфузія BNP, як внутрішньовенне введення ANP, 4,91 потужного та стійкого мобілізуючого ліпідного ефекту та підвищує рівень NEFA у плазмі крові, що може змінити роботу серця та протидіяти деяким корисним діям сполуки на інші тканини . Це все ще важливе та відкрите питання, і тому всі ліки, які, як відомо, активують залежні від NPR-A/-B шляхи, слід оцінювати на предмет їх метаболічних побічних ефектів.
Висновки
- Енн Хетеуей не рекомендувала втрачати вагу за роль Les Mis CTV News
- Антонія Кемпбелл-Хьюз Чому я голодую за цю роль London Evening Standard
- Огляд метаболічних ефектів контрольованого вивільнення фентермінтопірамату - PubMed
- Імунна система мозку може зіграти роль у збільшенні ваги Наукові новини для студентів
- Купити Метаболічний комплекс - 60 капсул - Ботанічний вибір