Хлорид
Хлорид виділяється в просвіт кишечника завдяки скоординованій дії базолатерального котранспортера Na +/2C1−/K + (NKCC1) та трансмембранного регулятора провідності апікального муковісцидозу (CFTR).
Пов’язані терміни:
- Бікарбонат натрію
- Неорганічні іони
- Секреція (процес)
- Білок
- Мутація
- Іон натрію
- Калій
- Кістозний фіброз
Завантажити у форматі PDF
Про цю сторінку
Харчування
Шеррі М. Льюїс,. Джозеф Дж. Кнапка, у лабораторному щурі (друге видання), 2006
ХЛОРИД.
Хлорид разом з натрієм та калієм відповідають за осмотичний тиск та кислотно-лужний баланс. Хлорид - найпоширеніший аніон у позаклітинній рідині. Як електронегативний елемент, Cl - це окислювач. На додаток до пасивної ролі в електролітному балансі, хлорид необхідний для виробництва соляної кислоти шлунка, що виділяється з тім’яних клітин слизової оболонки шлунка в шлунку (Groff and Gropper, 2000a). Ця слизова також виділяє пепсиноген, який активується HC1 і є внутрішнім фактором, необхідним для всмоктування вітаміну В12 та вироблення слизу. Слиз захищає орган від засвоєння HC1 та протеазами. HC1 діє як бактеріоцид, що запобігає переростанню шлунково-кишкового тракту від бактерій (Berdanier, 1998). Він також функціонує як обмінний аніон в еритроцитах для HCO - 3, відомий як зсув хлоридів. Цей процес дозволяє переносити СО2, отриманий з тканин, назад у легені (Groff and Gropper, 2000).
Орієнтовна харчова потреба в хлориді для щурів становить 0,5 г/кг дієтичного NRC (1995). Дефіцит хлориду у щурів розвивається повільно завдяки їх здатності зберігати електроліт, значно зменшуючи виведення сечі під час виснаження. Ознаками дефіциту хлоридів є поганий ріст, зниження ефективності годівлі, зниження вмісту хлориду в крові, зменшення виведення хлоридів та збільшення рівня NRC СО2 у крові (1995). Щури, яких годували дієтами, що містять високі концентрації хлоридів, росли нормально і мали нормальну концентрацію хлоридів у м’язах та нирках (Whitescarver et al., 1986; Kaup et al., 1991a, b). Однак щури Спраг-Доулі, які годували 15,6 г/кг харчового хлориду, мали підвищений артеріальний тиск і збільшення нирок (Kaup et al., 1991a, b). Котчен та ін. (1983) годували щурів Даля чутливими до солі 4,86 г/кг харчового хлориду, що призводило до підвищення артеріального тиску.
Природні атмосфери: корозія
1.2 Хлориди
Хлориди є особливо їдкими сполуками для багатьох металів. Розчинність у воді багатьох хлоридів металів відносно висока, і оскільки хлорид є одновалентним, він має тенденцію стабілізувати суспензоїдні золі, тим самим запобігаючи розвитку захисного шару продукту корозії. Хлориди знаходяться в морській воді у високій концентрації і, як правило, затримуються в повітрі під дією вітру на воду, що спричиняє прибій та бризки. Ці хлориди починаються як краплі морської води, але з часом вони висихають до дрібних твердих частинок. Як результат, регіони, що знаходяться поблизу океану, як правило, дуже їдкі для більшості металів, і корозійність є пропорційною близькості до прибою. Сталі та меншою мірою мідні сплави зазнають впливу хлориду, тоді як матеріали цинку та нікелю менше. У регіонах, дуже близьких до прибою, час вологості збільшиться, а також високі показники осадження хлоридів.
Осадження хлоридів можна виміряти за допомогою різних методів, але метод вологих свічок, ASTM G140, прийнятий як стандарт. Цей метод використовує обмотану марлею трубку, підтримувану вологою з водою, для захоплення або вологих, або сухих хлоридів. Після 30-денного впливу пристрій отримують і вимірюють вміст хлориду хімічним аналізом. Слід зазначити, що значення, отримані від хлоридної свічки, не обов'язково відповідають вимірам, отриманим за іншими геометріями колекції.
Хлориди також можна знайти в атмосфері поблизу автомагістралей та доріг, де натрій та/або хлорид кальцію використовуються для танення снігу та льоду взимку. У цих випадках спосіб транспортування полягає в розбризкуванні, а не в сухому нанесенні. Осадження дорожньої солі протягом багатьох років сприяло корозії та руйнуванню автомобільних компонентів.
ISO прийняв стандартну класифікацію осадження хлоридів. Ці значення наведені в таблиці 2. Вони базуються на вимірах вологих свічок і корисні для оцінки ділянок, розташованих ближче 1 км від джерела морської води.
Таблиця 2. Класи осадження хлоридів та діоксиду сірки на основі ISO 9223.
| S0 | 300 | P3 | > 81 | > 91 |
Швидкість осадження хлоридів на основі іона хлориду; Швидкість осадження SO2 на основі загальної сірки як SO2; Концентрація SO2 на основі SO2 при 25 ° C у повітрі при 1atm.
Молекулярно-клітинна біологія болю
5 Регулювання внутрішньоклітинних концентрацій аніонів
Регулювання хлоридів залежить від координації кількох процесів (рис. 2). Запропоновано певні канали витоку хлоридів для зменшення внутрішньоклітинної концентрації хлориду, діючи як односторонні клапани. Ця ідея випливає з спостереження, що хлоридні канали, такі як ClC-2 (ген clcn2), більш проникні для хлориду, що виходить з клітини, ніж для хлориду, що надходить у клітину. 35 Незалежно від цієї диференціальної проникності, яку називають випрямленням, напрямок хлоридного потоку все ще залежить від рушійної сили хлоридів. Це означає, що хлорид рідко, якщо коли-небудь матиме можливість вийти з клітини через ClC-2, оскільки хлоридна рушійна сила майже завжди знаходиться в протилежному напрямку. Оскільки "клапан" недосконалий, канали ClC-2 насправді пропускають хлорид у клітину. 36
Нездатність каналів випускати хлорид з клітини наголошує на необхідності різних механізмів транспорту іонів, які можуть рухати хлорид проти його градієнта. 37 Котранспортери, або симпотери, рухають два або більше видів іонів в одному напрямку по клітинній мембрані; хлорид може рухатися проти свого градієнта, переводячи ще один іон, який рухається вниз по його градієнту. Обмінники, або антипортери, роблять фактично те саме, але поєднуючи рух видів іонів, що протікають в протилежних напрямках через мембрану. Основним хлоридним екструдером у нейронах є калій-хлорид-котранспортер 2 (KCC2) (ген slc12a5). KCC2 пропускає хлоридні зворотні іони калію, які стікають по їх градієнту і виходять з клітини. Процес є електронейтральним завдяки стехіометрії хлориду та калію 1: 1. Процес неактивний, оскільки безпосередньо не включає гідроліз АТФ (і тому його не слід називати відкачуванням); натомість процес вторинно активний, оскільки KCC2 покладається на градієнт калію, який підтримується АТФ-азою натрій-калій, яка перекачує калій у клітину.
Як уже зазначалося, бікарбонат витікає через активовані ГАМКГ та гліцинові рецептори. Ймовірність витоку бікарбонату, що спричиняє позаклітинне накопичення, низька, враховуючи відносно необмежену дифузію бікарбонату в позаклітинний простір, але витік бікарбонату може виснажувати рівень внутрішньоклітинного бікарбонату та спричиняти падіння рН. 49 Однак це, як правило, не відбувається в звичайних умовах, оскільки внутрішньоклітинний бікарбонат поповнюється за рахунок перетворення вуглекислого газу та води в бікарбонат та протонів за допомогою ферменту карбоангідрази; як газ, вуглекислий газ вільно дифундує по клітинній мембрані. Внутрішньоклітинний бікарбонат може бути виснажений (і його витік таким чином скорочений) шляхом блокування карбоангідрази ацетазоламідом 32, який насправді може мати знеболюючий ефект (розділ 9). Регулювання рН включає інші хімічні реакції та транспортні механізми, а сам бікарбонат може бути переміщений по клітинній мембрані в обмін на хлорид. 50
Кілька ролей KCC2 у розвитку мозку
53.2.1 Білки CCC кодуються сімейством генів SLC12
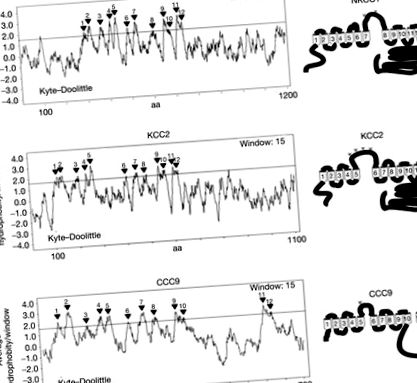
Білки CCC кодуються відповідними генами, які складають сімейство генів розчиненого носія 12 (SLC12) (таблиця 53.1) з дев'ятьма членами (Gamba, 2005). Прогнозується, що всі члени CCC (за винятком CCC9) мають 12 трансмембранних (TM) доменів (рис. 53.3); це експериментально підтверджено поки що лише для Na + –K + –2Cl - котранспортера 1 (NKCC1) (Gerelsaikhan and Turner, 2000; Gerelsaikhan et al., 2006).
Таблиця 53.1. Члени сім'ї CCC
| NKCC2 | SLC12A1 | Na +, K +, Cl - | 1099/178 | Гамба та ін. (1994) та Пейн та Форбуш (1994) |
| NKCC1 | SLC12A2 | Na +, K +, Cl - | 1191/262 | Дельпір та ін. (1994) та Xu та співавт. (1994) |
| NCC | SLC12A3 | Na +, Cl - | 1023/143 | Гамба та ін. (1993) |
| KCC1 | SLC12A4 | K +, Cl - | 1085/123 | Гіллен та ін. (1996) |
| KCC2 | SLC12A5 | К + , Кл - | 1116/104 | Пейн та ін. (1996) |
| KCC3 | SLC12A6 | K +, Cl - | 1150/190 | Хікі та ін. (1999), Mount et al. (1999) та Race et al. (1999) |
| KCC4 | SLC12A7 | K +, Cl - | 1083/123 | Маунт та ін. (1999) |
| CCC9 | SLC12A8 | Невідомо | 714/44 | Хьюетт та ін. (2002) |
| CIP | SLC12A9 | Невідомо | 915/44 | Карон та співавт. (2000) |
Малюнок 53.3. Графіки гідропатії для білків NKCC1, KCC2 та CCC9. Аналіз гідропатії Кайта – Дуліттла (ліворуч із використанням вікна 15 аа (Kyte and Doolittle, 1982)) пропонує домени 12-TM для NKCC1 (a), KCC2 (b) і, можливо, також для CCC9 (c). Схематичні моделі білків NKCC1 (a), KCC2 (b) та CCC9 (c) з 12 сегментами TM представлені праворуч.
Сімейство CCC поділяється на три гілки (рис. 53.4). Перша гілка включає Na + -залежний K + –Cl - котранспортери NKCC1 та NKCC2, а також Na + -залежний Cl - котранспортер NCC. Ці білки опосередковують електронейтральний Na + -приведений Cl - транспорт, незалежно від їх використання K +, і діляться
55% гомологія в амінокислотних послідовностях. Друга гілка включає чотири K + -залежні Cl - котранспортери KCC1, KCC2, KCC3 і KCC4, які опосередковують електронейтральний K + -парний Cl - транспорт і спільне використання
70% амінокислотної ідентичності. На відміну від цього, члени цих двох відділень CCC є лише приблизно на 25% гомологічними між собою. Третя гілка CCC представлена двома членами-сиротами CCC - катіон– хлоридним транспортером 9 (CCC9) та CCC-взаємодіючим білком 1 (CIP1), які демонструють лише
20–25% ідентичності з іншими ССС (Gamba, 2005).
Малюнок 53.4. Філогенетичне дерево сімейства CCC. На сьогодні сімейство CCC (затінене зеленим) поділено на три гілки, що представляють членів N (K) CC, KCC та сиріт. Outgroup представлений трьома членами сім'ї SLC7. Аналіз філогенетичного дерева проводили за допомогою програми ClustalW Tree (Biology Workbench). Значення Bootstrap (відсоток того, як часто кожна гілка представлена у всіх деревах з перепробором), вказуються біля гілок. Довжина гілок відповідає середній кількості амінокислотних заміщень на сайт у вирівняних послідовностях. Смужка шкали відповідає 0,1 заміни на сайт.
КЛІНІЧНИЙ АНАЛІЗ | Електроліти у фізіологічних зразках
Значення та інтерпретація результатів
Вимірювання концентрації хлоридів у сироватці крові (таблиця 1) має значення у випадку нормальної концентрації води у зразку. При гіперліпемії або гіперпротеїнемії відбувається «згруповане», оскільки збільшення, наприклад, на 10% у відділенні, що містить макромолекули, зменшує концентрацію хлориду на 10%. Зсув на 10% особливо важливий, коли контрольний інтервал порівняно невеликий. У випадку хлоридів верхня межа контрольного інтервалу відрізняється від нижньої межі на 11% (див. Натрій вище). Тому концентрацію хлоридів у сироватці крові слід коригувати (див. Значення та інтерпретація результатів вище), коли концентрація води ненормальна, щоб бути порівнянною з контрольним інтервалом.
Аніонний зазор (AG) (ммоль l -1) розраховується як
де [Na +] - концентрація натрію в сироватці крові (ммоль l -1), [Cl -] - концентрація хлоридів у сироватці крові (ммоль l -1), а [HCO3 -] - концентрація гідрогенкарбонату в сироватці крові (ммоль l -1).
Опорний інтервал аніонної щілини становить від +8 до +16 ммоль l -1. Розрив обумовлений тим, що сума катіонів (наприклад, K +, Ca 2+), яка не враховується, нижча за суму аніонів, які виключені з розрахунку (білки, органічні кислоти) . Аніонна щілина збільшується у випадках діабетичного кетоацидозу, лактатацидозу та певних інтоксикацій саліцилатом, метанолом (форматом), етанолом (лактатом) та етиленгліколем (оксалат, гліколат, гліоксилат). Аніонний зазор зменшується або навіть стає негативним у разі високих концентрацій броміду, особливо якщо концентрація хлоридів визначається методом, який є більш чутливим до броміду, ніж до хлориду.
Концентрація натрію та концентрація хлоридів, як правило, змінюються в одному напрямку та в однаковій мірі, тоді як хлорид та гідрокарбонат змінюються взаємно (Таблиця 4).
Таблиця 4. Порушення хлоридного балансу
| 1 | Гіпохлоремія | |
| 1.1 | Причина: недостатнє споживання хлориду | |
| 1.2 | Причина: Втрата хлориду | |
| Приклади: | Блювота | |
| Промивання шлунка | ||
| Метаболічний алкалоз | ||
| Респіраторний ацидоз | ||
| Діуретики | ||
| 1.3 | Причина: Гіпотонічна дегідратація (див. Натрій) | |
| 1.4 | Причина: Гіпотонічна гіпергідратація (див. Натрій) | |
| 2 | Гіперхлоремія | |
| 2.1 | Причина: надмірне введення хлориду | |
| Приклади: | Інфузія великої кількості хлориду | |
| Уретеросигмоїдостомія | ||
| 2.2 | Причина: Зниження елімінації хлориду | |
| (через втрату карбонату водню) | ||
| Приклади: | Діарея | |
| Свищ підшлункової залози | ||
| Канальцевий ацидоз нирок | ||
| Гіпоальдостеронізм з ацидозом | ||
| 2.3 | Причина: гіпертонічна дегідратація (див. Натрій) | |
| 2.4 | Причина: гіпертонічна гіпергідратація (див. Натрій) | |
Змінено з Külpmann WR, Stummvoll HK та Lehmann P (1996) Електроліти: клінічні та лабораторні аспекти. Нью-Йорк: Спрінгер.
Виділення хлориду з сечею (табл. 3) зазвичай нагадує виведення натрію. У разі метаболічного алкалозу внаслідок надниркової втрати хлориду екскреція хлориду становить -1. Якщо метаболічний алкалоз викликаний надлишком мінералокортикоїдів, екскреція хлориду не впливає і становить> 10 ммоль d -1 .
Різноманітність та функції рецепторів ГАМК: Вшанування Ганна Мелера, частина Б
3.2.2 Генетично кодовані датчики хлоридів
Хлоридна візуалізація не може виявити ні маневрового гальмування, ні бікарбонатного потоку, і тому дозволяє лише опосередковані твердження про вплив GABA-ергічного сигналу на збудливість постсинаптичного нейрона.
Біохімічні параметри в токсикологічних дослідженнях в Африці
23.5.3 Хлорид
Анатомія та фізіологія тонкого і товстого кишок
Секреція
У клубовій кишці та товстій кишці NHE та Cl -/HCO3 - обмінники в апікальних мембранах виробляють чисте електронейтральне поглинання NaCl та секрецію H + HCO3 -. Подвійна дія білків DRA (SLC26A3) та PAT1 (SLC26A6) виробляє електронейтральну секрецію HCO3 - та поглинання Cl -. Хлорид-незалежні механізми секреції бікарбонату включають цАМФ-залежну секрецію та HCO3 - секрецію, пов’язану з поглинанням коротколанцюгових жирних кислот. 84
- Агент проти ожиріння - огляд тем ScienceDirect
- Апітерапія - огляд тем ScienceDirect
- Бета-лактоглобулін - огляд тем ScienceDirect
- Хвороба жовчних шляхів - огляд тем ScienceDirect
- Аргінін - огляд тем ScienceDirect