Ефективність рідкої низькоенергетичної дієти для досягнення передопераційної цільової втрати ваги перед баріатричною операцією
Самотній В. Нільсен
1 Кафедра харчування, фізичних вправ і спорту, Факультет наук, Університет Копенгагена, Данія
Метте С. Нільсен
1 Кафедра харчування, фізичних вправ і спорту, Факультет наук, Університет Копенгагена, Данія
Джулі Б. Шмідт
1 Кафедра харчування, фізичних вправ і спорту, Факультет наук, Університет Копенгагена, Данія
Сью Д. Педерсен
1 Кафедра харчування, фізичних вправ і спорту, Факультет наук, Університет Копенгагена, Данія
2 Ендокринологічна клініка C-ENDO, Калгарі, АБ, Канада
Андерс Сьодін
1 Кафедра харчування, фізичних вправ і спорту, Факультет наук, Університет Копенгагена, Данія
Анотація
Передопераційна втрата ваги на 8% є необхідною умовою для проведення баріатричної хірургії (BS) в Данії. Метою цього дослідження було оцінити ефективність 7- або 11-тижневої дієти з низьким енергоспоживанням (РК) для досягнення передопераційної цільової ваги перед БС. Загалом тридцять пацієнтів із ожирінням (ІМТ 46 · 0 (sd 4 · 4) кг/м 2) стежили за РК (Кембриджський план ваги ®, 4184 кДж/добу (1000 ккал/д)) протягом 7 або 11 тижнів як підготовка до BS. Антропометричні вимірювання, включаючи склад тіла (двоенергетична рентгенівська абсорбціометрія), параметри крові та артеріальний тиск оцінювали на тижнях 0, 7 та 11. На 7 тижні більшість пацієнтів (77%) досягли цільової ваги, і це було досягнуто через 5,4 (семи 0,03) тижнів. Середня втрата ваги становила 9,3 (сім 0,05)% (P sem 2 · 3) та 7 · 3 (sem 1,8 ·) мм рт. Ст., Відповідно, усі P sem 1 · 8)% зменшення глюкози натще (P sem 6 · 4)% зниження інсуліну натще (P sem 2 · 2)% зменшення LDL (P sem 4 · 7)% зменшення TAG (P Ключові слова: Низькоенергетичні дієти, рідкі дієтичні суміші, передопераційне схуднення, баріатрична хірургія
Єдиним довготривалим ефективним лікуванням, яке в даний час доведено подолати важке ожиріння, є баріатрична хірургія (БС) (, 1). Дослідження показали, що складність хірургічної процедури та ризик післяопераційних та післяопераційних ускладнень пов'язані зі ступенем ожиріння (, 2, 3) .
Переваги передопераційної втрати ваги включають зменшення ризику періопераційних ускладнень за рахунок зменшення вісцеральної жирової тканини та вмісту внутрішньопечінкового жиру, тим самим мінімізуючи ризик переходу на відкриту операцію (, 2, 4 - 6), скорочення операційного часу (, 7 - 10), а також тривалість госпіталізації (, 10, 11). Крім того, передопераційна втрата ваги може бути пов’язана навіть із поліпшенням післяопераційної втрати ваги (, 7, 10, 11), потенційно відображаючи мотивацію пацієнтів, а також привчаючи пацієнтів до обмеженого харчування після операції. Тому, щоб оптимізувати безпеку та ефективність БС у пацієнтів з важким ожирінням, передопераційна втрата ваги є кращою.
Більшість хірургів радять пацієнтам худнути до перенесеного захворювання. Міністерство охорони здоров'я Данії вимагає зниження ваги на 8% для пацієнтів, яких планують на БС (, 12); однак наразі не встановлено стандартної дієтичної програми для отримання передопераційної цільової ваги. Втрата ваги, досягнута за допомогою звичайної дієти та змін способу життя, може бути дуже важкою для деяких пацієнтів, особливо заздалегідь визначений час. У таких випадках ефективним варіантом може бути дієта з низьким енергоспоживанням (РК) з високим вмістом білка. Ці формули зазвичай обмежують споживання енергії до 3347–6276 кДж/день (800–1500 ккал/день), але містять усі основні поживні речовини. Низькоенергетичні високобілкові суміші здатні спричинити швидку втрату ваги, часто забезпечують відносно адекватне насичення через кілька днів і намагаються мінімізувати втрату нежирної маси (FFM) (, 13, 14). Оскільки щорічно в усьому світі проводиться понад 300 000 процедур BS ((15), це посилює необхідність досліджень з акцентом на вдосконалення передопераційних стратегій схуднення.
У цьому дослідженні ми мали на меті визначити ефективність РК для досягнення 8% втрати ваги у пацієнтів з важким ожирінням до БС. По-друге, були оцінені потенційні переваги для здоров'я та побічні ефекти РК.
Методи
Це дослідження було частиною більш широкого дослідження; детальний опис методів нещодавно був опублікований в інших місцях (, 16) .
Навчання населення
Загалом тридцять кавказців у віці 18–65 років з ІМТ ≥ 40 або ІМТ ≥ 35 кг/м 2 у поєднанні з обструктивним апное сну або гіпертонічною хворобою, затвердженими для шлункового шунтування Roux-en-Y, були набрані з листопада 2009 року по серпень 2011 року. критерії були або пов'язані з кінцевими точками в основному дослідженні і включали цукровий діабет, дисфункцію щитовидної залози, гіпоталамічну або генетичну етіологію ожиріння (, 16), або протипоказання, пов'язані з використанням ЖК: попередній випадок дивертикуліту, минула історія шлуночкових аритмій, ниркова дисфункція (кліренс креатиніну 3 × верхня межа норми), алергія на молочний білок або непереносимість лактози, порфірія або фенілкетонурія, подагра в анамнезі, годування груддю, одночасне застосування інгібіторів моноаміноксидази або некалієзберігаючих діуретиків, або нездатність або небажання дотримуватися з РК-дисплеєм.
Це дослідження було проведено відповідно до керівних принципів, викладених у Гельсінській декларації, і всі процедури, що стосуються суб'єктів людського життя, були затверджені Муніципальним етичним комітетом Копенгагена/Науковим комітетом з етики столичних регіонів Данії (журнал № H-2-2009- 091), Датським агентством із захисту даних (журнал № 2007-54-0296) та було зареєстровано за адресою kliničkitrials.gov (ClinicalTrials.gov ID> NCT00939679). Письмова інформована згода була отримана від усіх суб’єктів.
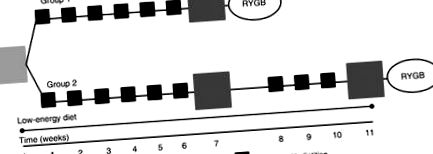
Дослідження включало базовий візит (тиждень 0) та два подальші візити на 7 та 11 тижнях. Щоб дослідити вплив на первинну кінцеву точку основного дослідження (енергетичні витрати) (, 16), випробовуваних було рандомізовано до одного з дві групи: група 1, запланована на шунтування шлункового шунтування Roux-en-Y на 8 тижні (n 15), або група 2, запланована на шунтування шлункового шунтування Roux-en-Y на 12 тиждень (n 15). Усі учасники отримали РК-дисплей протягом 11 тижнів. У цій роботі будуть досліджуватися лише доопераційні періоди: тобто період з 0 по 7 тиждень (включаючи обидві групи 1 і 2, n 30) і період з 7 по 11 тиждень (лише група 2, n 15) ( Рис. 1). Випробовувані щотижня отримували дієтологічні консультації з питань харчування.
Огляд проекту дослідження. Оскільки основним дослідженням було контрольоване дослідження, учасників рандомізували на операцію шлункового шунтування (RYGB) Roux-en-Y на 8 тижні (група 1) або на 12 тижні (група 2). Учасники дотримувались дієти з низьким енергоспоживанням з 0 по 11 тиждень.
Скринінг
Пацієнти, які мають право на дослідження, були визначені ендокринологами в лікарні Hvidovre, Копенгаген, Данія, і скеровані на скринінговий візит у Департамент харчування, фізичних вправ та спорту Університету Копенгагена, де були пояснені деталі протоколу та призначено базовий візит.
Базовий рівень (тиждень 0) та подальші візити (тижні 7 та 11)
Під час базового візиту були отримані демографічні дані та історія хвороби, і пацієнти були рандомізовані на хірургічне втручання або на 8, або на 12-му тижні. Антропометричні дані були зібрані, відібрана проба крові натще, а частота серцевих скорочень та артеріальний тиск вимірювались у тих, хто відпочивав та знаходився в лежачи на спині. ЖК було розпочато з першого візиту до дієтолога.
Базовий візит та два наступних візити були однаковими.
Низькоенергетична дієта
РК складався з чотирьох страв на основі порошку (Cambridge Weight Plan ®), 1 літра знежиреного молока, 295 г овочів та 100 г нежирного йогурту на добу, забезпечуючи 4310 кДж/день (1030 ккал/день) (48% енергії ( E%) від вуглеводів, 39 E% від білка, 13 E% від жиру та ≥100% рекомендованих добових доз усіх вітамінів та мінералів). Під час щотижневої зустрічі з дієтологом реєстрували самооцінку побічних ефектів та відповідність РК. Відповідність оцінювали за шкалою від 1 до 5, при цьому 5 означала "дуже хороша відповідність".
Антропометричні вимірювання
Випробовуваних поінформували про те, що вони повинні носити легкий одяг, не мати взуття, мати спорожнений сечовий міхур та голодуватись для антропометричної оцінки. Вагу тіла вимірювали з точністю до 0,1 кг. Окружність талії та стегон вимірювали двічі з точністю до 0,5 см і використовували середнє значення. Висоту вимірювали з точністю до 0,5 см за допомогою настінного цифрового стадіометра. Склад тіла визначали за допомогою двоенергетичної рентгенівської абсорбціометрії (DXA). Вимірювання DXA проводили за допомогою сканування половини тіла (, 17). Протягом усього дослідження використовувався той самий сканер DXA (Lunar Prodigy, версія програмного забезпечення Encore 12.3), щоб уникнути змін в аналізі результатів сканування. Однак через обмеження ваги три об'єкти були відскановані в сканері DXA із більшим розміром таблиці та вагомістю (Lunar iDXA, версія програмного забезпечення Encore 12.3).
Біохімічні заходи
Зразки крові збирали протягом ночі швидко (10–12 год) та аналізували на вміст глюкози, інсуліну, С-пептиду, TAG, загального холестерину, ЛПВЩ, ЛПНЩ та високочутливого С-реактивного білка. Підготовка та аналіз зразків крові були детально описані в інших місцях (, 16). CV у межах та між результатами аналізу були нижче 3,5 та 6,5% відповідно для всіх біохімічних показників.
Статистичний аналіз
Усі статистичні аналізи проводились у версії R 2.14.0 (www.r-project.org).
Описові зведення даних (вік, маса тіла, ІМТ) представлені як середні значення та стандартні відхилення. Ефективність РК для всіх кінцевих точок моделювалася у змішаній лінійній моделі з тижнем як фіксованим ефектом та предметом як випадковим ефектом. Всі аналізи базувались на намірі для лікування з базовими спостереженнями, перенесеними для відсутніх даних (n 2), за винятком маси тіла, де останнє спостереження (виміряне на щотижневій зустрічі з дієтологом) було перенесено для відсутніх даних. Субаналізи моделювались у змішаній лінійній моделі, що включала тижневу × групову взаємодію та з суб’єктом як випадковий ефект. Дані представлені як середні значення зі стандартними похибками.
Значення P відповідають тестам коефіцієнта ймовірності та значенням P (, 16). Однак розрахунок обсягу вибірки, заснований на даних попереднього дослідження з використанням РК-дисплея 3347–4184 кДж (800–1000 ккал) протягом 8 тижнів (, 18), показав, що завдяки нашому обсягу вибірки нам вдалося виявити вагу 8% втрата у осіб із ожирінням (що відповідає середній втраті ваги 11 · 1 кг, sd 3,3 кг і мінімальній відповідній різниці 8 кг (8% втрати ваги); α = 0,05, β = 0 · 8 ).
Результати
Описові дані
Загалом у дослідження було включено вісім чоловіків та двадцять дві жінки. Середній вік становив 38 · 8 (sd 10 · 4) років, із середньою масою тіла на вихідному рівні 135 · 1 (sd 19 · 2) кг та ІМТ 46 · 0 (sd 4 · 4) кг/м 2. Два суб'єкти кинули навчання до першого подальшого візиту (7 тиждень) через особисті проблеми та неможливість дотримання вимог РК.
Втрата ваги
Середня втрата ваги на 7 тижні становила 9,3 (сім 0,05)%, що відповідає втраті ваги 12,7 (сім 0,08) кг (рис. 2).
Щотижнева втрата ваги (%), виміряна з 0 по 7 тиждень (n 30; групи 1 та 2; ○) та з 0 до 11 тижня лише у групі 2 (n 15; X). Група 1 була оперована на 8 тижні; група 2 була оперована в тиждень 12. Значення є середніми, стандартні похибки представлені вертикальними смугами.
Із включених пацієнтів 77% досягли своєї передопераційної цільової ваги, і це в середньому було досягнуто на 5–4 тижні (на 0,03). Втрата ваги в групі, яка досягла цільової ваги до 7 тижня (n 23), становила 10,2 (сім 0,03)%, що відповідає зменшенню ваги на 14,1 (семи 0,07) кг, тоді як середня втрата ваги для решти суб’єктів на 7 тижні (n 7) становило 6 · 1 (сім 0,9)%, що відповідає зменшенню ваги на 7 · 9 (сім 1,2 ·) кг. Відсоток втрати ваги на 7 тижні не передбачав відсотка надмірної втрати ваги через 18 місяців після операції (r −0 · 40; P = 0 · 07).
Подальше зниження маси тіла на 3,9 (семи 0,05)% спостерігалося з 7 по 11 тиждень у п’ятнадцяти пацієнтів, призначених на БС на 12 тижні (P sem 0 · 1) з 0 по 7 тиждень, і залишалося незмінним до тиждень 11 (4 · 1 (сім 0 · 2); Р = 0 · 16). Відповідність позитивно асоціювалась із відсотковою втратою ваги з 0 по 7 тиждень (r 0,59; P sem 0,88) та 2,3 (sem 0,77%, відповідно) спостерігалося з 7 по 11 тиждень (обидва P sem 0 · 5) проти 8,7 (сім 0,7)%; P sem 1 · 0) та 3 · 5 (sem 0 · 7) кг відповідно, рис.3).
FFM, нежирна маса; FM, жирова маса; hs-CRP, високочутливий С-реактивний білок; АТ, артеріальний тиск; ЧСС, частота серцевих скорочень.
Середнє значення зміни з 0 по 7 тиждень було значущим: * P sem 1 · 3) уд/хв, 7 · 1 (sem 2 · 3) та 7 · 3 (sem 1 · 8) мм рт. Ст., Відповідно (всі P 140/90 мм рт.ст.), і лише один із цих пацієнтів був фармакологічно пролікований для цього. Артеріальний тиск нормалізувався у п'яти з цих шести пацієнтів на 7 тижні. Ще п'ять пацієнтів отримували антигіпертензивні препарати з артеріальним тиском у межах норми на початковому рівні. Лікування було скасовано у одного з цих пацієнтів на 7 тижні.
Побічні ефекти
Найчастіше повідомлялося про побічні ефекти: головний біль, втома, запор, запаморочення та інфекції верхніх дихальних шляхів (про це повідомляли 57, 50, 43, 33 та 30% відповідно). Інші менш відомі побічні ефекти включали непереносимість холоду, голод, біль у животі, дратівливість, сухість шкіри, діарею, метеоризм та неприємний запах з рота. Про серйозні побічні явища не повідомлялося.
Обговорення
Оскільки дієтологічне консультування є важливим аспектом лікування ожиріння (, 35, 36), обмеження цього дослідження полягає в тому, що результати можуть не застосовуватися безпосередньо до кандидатів на БС, які не отримують щотижневих консультацій з питань харчування та заохочення від досвідчених медичний працівник. Крім того, виключення хворих на цукровий діабет та суб'єктів, які не бажали дотримуватися РК, могло вплинути на наші результати, оскільки ця група може бути менш схильна до втрати ваги (, 37). Іншим обмеженням є DXA, який не був повністю оцінений як інструмент оцінки складу тіла у пацієнтів з важким ожирінням, і повідомлялося, що він не надає достовірних даних при динамічній втраті ваги через неточні припущення про постійну гідратацію FFM (, 38) .
На закінчення, наші результати свідчать про те, що можна отримати передопераційну втрату ваги на 8% за допомогою РК-дисплея протягом 7 тижнів. Втрата ваги на 7-му тижні супроводжувалася поліпшенням метаболічного профілю та зниженням артеріального тиску, без подальших поліпшень після додаткової втрати ваги на 3,9% на 11-му тижні. Механізми надмірного зменшення ЖЖ у пацієнтів із високим ожирінням РК потребує подальших досліджень, включаючи потенціал для оптимізації РК-формул, що використовуються для того, щоб обмежити втрату метаболічно активної тканини.
Подяки
Автори дякують Luise Gunvald MSc, John Gargul Lind BSc, Lene Stevner MSc, Jane Jørgensen BSc, Søren Andresen BSc, Marianne Juul BSc, Ulla Skovbæch Pedersen BSc, Department of Nutrition, Exercise and Sports, Denmark.
Дослідження було проведено в рамках UNIK: Food, Fitness and Pharma for Health and Disease в Університеті Копенгагена. Проект UNIK фінансувався Міністерством науки, технологій та інновацій Данії, грант № 09-065308. Продукти з низьким енергоспоживанням були надані Cambridge Weight Plan ® (Корбі, Нортантс, Великобританія). UNIK та Cambridge Weight Plan ® не мали жодної ролі в розробці, аналізі чи написанні цієї статті.
Розроблені дослідження: А. С. та С. Д. П.; скоординований збір даних: J. B. S., L. V. N. та M. S. N .; проаналізовані дані: Л. В. Н. та М. С. Н .; обговорювали аналіз та інтерпретацію даних: Л. В. Н., М. С. Н., Дж. Б. С., С. Д. П. та А. С .; написали роботу: Л. В. Н. та М. С. Н .; несла основну відповідальність за остаточний зміст: А. С .; всі автори критично переглянули рукопис і затвердили остаточний рукопис.
J. B. S., M. S. N. та L. V. N. отримали гранти на подорожі від Cambridge Weight Plan ®. Продукти з низьким енергоспоживанням були надані Cambridge Weight Plan ®. UNIK та Cambridge Weight Plan ® не мали жодної ролі в розробці, аналізі чи написанні цієї статті.
- Ден Стівенс Втрата ваги, дієта та фотографії
- Вплив дозволеного вибору дієти на схуднення Рандомізоване дослідження - PubMed
- Вибирайте дієтичну їжу для схуднення, корисні соки, органічний мед - ZOE
- 10-денна дієта Даніеля - Йорданія Рубін (овочі, фунти, тренування, сіль) - Дієта та схуднення
- FDA затверджує новий гель для схуднення Огляди середньої втрати ваги за 30-денну кето-дієту