Антигістамінний препарат "супрастин"
Винахід відноситься до медицини, зокрема до препарату антигістамінної дії. Запропонований антигістамінний препарат, виготовлений у формі таблеток і містить в якості активного інгредієнта хлорпіраміну гідрохлорид у кількості 10-15% від ваги таблетки, а також як допоміжні речовини кукурудзяний крохмаль, амілопектин, тальк, желатин, стеарат магнію та лактозу, в той час як масова частка допоміжних речовин від масової частки основної діючої речовини становить: кукурудзяний крохмаль - 1,5-2,5 амілопектин - 0,05-0,1 тальк - 0,2 желатин - 0,01-0,06 стеарат магнію 0, 12 Лактоза - залишок препарату завдяки відбору допоміжних інгредієнтів та їх кількісному співвідношенню покращує распадаемість та розчинність, що позитивно проявляється при введенні в терапевтичних цілях. 3 табл., 2 іл.
Винахід відноситься до галузі медицини і стосується отримання лікарського засобу, який містить як діючу речовину хлорпіраміну гідрохлорид і має антигістамінну, протиалергічну дію.
Хлоропірамін є блокатором гістамінергічних реакцій. Крім протиалергічного заспокійливого і виражений протисвербіжний ефект. Володіє периферичною антихолінергічною активністю, помірними запальними властивостями.
Широке використання антагоністів рецепторів гістаміну 1-го типу (рецептори Н1) як протиалергічних засобів виявило вирішальну роль цього медіатора в механізмі більшості симптомів алергічних захворювань.
Історія створення Н1-антигістамінних препаратів є прикладом науково обґрунтованого пошукового фармакологічного контролю однієї з найважливіших форм патології людини. Таким чином, найважливішими були наступні події.
На початку XX століття відбувся синтез гістаміну з імідазолінонової кислоти. У той же час гістамін витягували з ріжків і продемонстрували його освіту з гнильних гнильних бактерій за участю декарбоксилази. Потім встановили фармакологічну дію гістаміну на вищих тварин і обґрунтували його фізіологічну функцію медіатора.
До 20 років доведена роль гістаміну як медіатора алергічних реакцій: анафілактичний шок, риніт, бронхіальна астма, ХР є основною діяльністю. П'ять років потому з'явилися перші антигістамінні препарати, застосовні до людей (фінансами, піриламін малеат). Це був період широкого клінічного використання цього класу препаратів.
У 60-ті роки були отримані докази неоднорідності клітинних рецепторів гістаміну, представлених щонайменше двох типів: H1і H2-рецепторів. Було продемонстровано, що клінічні прояви алергії опосередковані головним чином дією гістамінових Н1-рецепторів, а антиалергічний ефект відомих антигістамінних препаратів пов'язаний з блокадою Н1-рецепторів.
В кінці 70-х років були отримані від представників антигістамінних препаратів, які мають більш високу спорідненість до рецепторів Н1 і практично не мають седативних препаратів 2-го покоління.
Нові препарати 2-го покоління не означає повної заміни їх препаратів 1-го покоління з наступних причин. Важливим фактором, що обґрунтовує широке клінічне використання антагоністів H1 1-го покоління, є багатий медичний досвід їх застосування і, відповідно, детальне знання їх Fermi 1-го покоління на додаток до рецепторів гістаміну та деяких інших медіаторів, хоча це може бути причина окремих побічних ефектів, однак при обгрунтованому використанні дозволяє поширити терапевтичний ефект, зокрема, через блокаду 5-гідрокситриптаміну (серотоніну).
Седативна дія ліків 1-го покоління може бути корисною для усунення ряду супутніх симптомів алергії, зокрема, для зменшення почуття свербежу, що посилюється вночі, та нормалізації порушеного сну.
Відносна короткочасна дія блокаторів N1-гістамінових рецепторів 1-го покоління дозволяє використовувати дробові дози та поєднувати один антагоніст H1 з іншим, включаючи препарати 2-го покоління.
Нарешті, суттєвою є відносно низька вартість цих препаратів, значно менша, ніж вартість 2-го покоління. У сучасних умовах цей фактор іноді є домінуючим, враховуючи необхідність тривалого застосування антигістамінних препаратів пацієнтам з алергічними захворюваннями.
Хлоропірамін застосовується при лікуванні алергічних захворювань різного походження, а також у косметичних препаратах (заявка JP 19960185923, a 61 K 7/00, 1996).
Відома таблетка, що містить хлоропірамін і отримана шляхом змішування, є етиленгліколем і оксипропіляцією в ізопропіловому спирті. SU 1577684, 61 K 20 вересня 1984 р.).
Найбільш близьким за технічною сутністю і досягнутим результатом є препарат "Супрастин" у формі таблеток по 25 мг (Машковський М. Д. Ліки, Москва, 1993, Х. 1, С. 354).
Мета цього винаходу забезпечити внутрішню стабільність під час зберігання таблеток на основі хлоропіраміну з розчинністю та розпаданість покращена за рахунок підбору допоміжних інгредієнтів та їх кількісного співвідношення. Для вирішення проблеми та досягнення технічного результату запропоновано антигістамінний засіб під назвою «Супрастин». Він виготовляється у формі таблеток і містить як діючу речовину хлоропіраміну гідрохлорид у кількості 10-15% від ваги таблетки. В якості допоміжних речовин препарат включає кукурудзяний крохмаль, амілопектин, тальк, желатин, стеарат магнію та лактозу. Масова частка допоміжних речовин від масової частки основної діючої речовини становить: кукурудзяний Крохмаль - 1,5-2,5 Амілопектин - 0,05-0,1
Тальк - 0,2
Желатин - 0,01-0,06
Стеарат магнію - 0,12
Лактоза - відпочинок
Приклад. Таблетки "Супрастин" 25 мг
Склад одна таблетка, 046
Амілопектин - 0,002
Тальк - 0,006
Желатин - 0,001
Стеарат магнію - 0,003
Хлоропіраміну гідрохлорид змішують з допоміжними речовинами, суміш гранулюють, сушать, просівають, оптиву і таблетують. Отримайте таблетки "Супрастин білого або сірувато-білого кольору, обличчя, фаски, без або майже без запаху. Вага таблеток 0,2 г
Дослідження експериментального препарату - таблетки "Супрастин" 25 мг у порівнянні з таблетками "Супрастин" 25 мг фірми "Чорне око", Угорщина.
Для визначення спектра поглинання порівняних препаратів був використаний спектрофотометр Ultrospec II "виробничої компанії" LKB Biochrom ". На фіг. 1 і 2 представлений огляд спектрів поглинання розчинів таблеток експериментального препарату та препарату-компаратора. Як можна бачити, спектри поглинання досліджуваних та контрольних препаратів абсолютно однакові.Оптична активність спостерігається в інтервалі довжин хвиль від 200 до 350 нм. Є три пікові поглинання на довжинах хвиль 222, 244, 306 нм і три виражені мінімальні поглинання на довжинах хвиль 212, 233, 274 нм. В області довжин хвиль понад 340 нм оптична щільність монотонно зменшується до нуля.
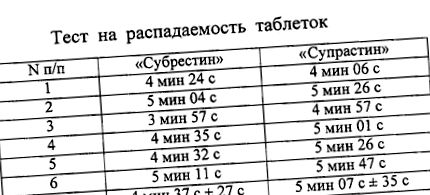
Дослідження распадаемості препаратів "Супрастин і Супраст" повторного процесу розподілення типу "розгойдується кошик" виробничої компанії "Ервека". Результати наведені в таблиці. 1. Час розподілення препарату на таблетки "Супрастин" становило 4 хв. 37 27, а на таблетки "Супрастин" "- 5 хв. 7 35 с. У всіх випадках час розпадуемості як досвідчених таблеток і таблеток порівняння становило від 4 до 6 хв, що значно менше, ніж нормальний GF (не більше 15 хвилин).
Визначення розчинення проводили на пристрої типу "поворотний кошик" виробничої компанії "Erweka". Як видно з наведеної таблиці. 2 результати через 45 хв розчинення таблеток "Супрастин" у розчині пройшло (91 4,2)% активного запуску та таблеток "Супрастин" - (89 4,1)%.
Порівняльна оцінка гострої та підгострої токсичності препаратів "Супрастин та Супрастин".
Для визначення гострої токсичності використовували безпородних мишей масою 17-23 г кожна. Суспензійні препарати, приготовані на основі 3% розчину крохмалю, вводили мишам per os через зонд в обсязі 1,0 мл.
Всім було використано 72 нелінійних миші, розділених на шість груп по шість тварин у кожній. Досвідчений препарат та препарат порівняння вводили у дозах 200, 400, 600, 800 та 1000 мг/кг
Обидва суб'єкти дози піної 1000 мг/кг, тобто виявилися низькотоксичними. Дози 1000 мг/кг були повністю портативними, вони більш терапевтичні (8 мг/кг) у 125 разів.
Підгостра токсичність досліджуваних препаратів у безпородних щурів масою 180-220 г кожен. Препарати вводили внутрішньошлунково в обсягах і розведеннях, зазначених у табл. 3. Враховуючи те, що терапевтична доза 8 мг/кг та десятикратна терапевтична доза 80 мг/кг, лабораторних тварин розділили на п’ять груп:
група 1 - 10-разова терапевтична доза «Супрастин»;
2 група - терапевтична доза препарату «Супрастин»;
група 3 - 10-разова терапевтична доза «Супрастин»;
4 група - терапевтична доза препарату «Супрастин»;
група 5 - цілі тварини, оброблені фізіологічним розчином.
Тривалість введення препарату становила 14 днів. Під час експерименту ступінь інтоксикації оцінювали за загальним станом тварини, станом шерсті, зміною кількості уріатів, дефекацією, слиновиділенням, початком тремору, судом, зміною частоти та ритму дихання.
Після введення наркотиків проводиться забій тварин і їх посмертне з подальшим взвешиванием лесенки, тимусу і головного мозку. Крім того, в крові тварин були виявлені такі біохімічні та гематологічні показники, як загальний білок, глюкоза, сечовина, активність аланінтрансфери (ALT), аспартокіназа (ACT), лужна фосфатаза, концентрація гемоглобіну, тромбоцити та лейкоцити.
За весь час адміністрації не повідомлялося про смертельну аварію. Обидва препарати як терапевтичні та 10-кратні терапевтичні дози не викликали статистично значущих відхилень у масі внутрішніх органів чи інших видимих ознак інтоксикації.
При визначенні вмісту загального білка, глюкози, сечовини, активність як трансаміназ, так і лужної фосфатази в плазмі крові лабораторних тварин різниці в результатах біохімічного аналізу між досліджуваним препаратом та препаратом-компаратором також не позначається використання терапевтичних доз або при використанні 10-кратної терапевтичної дози. Крім того, відсутні статистично значущі відмінності між цими результатами та результатами, отриманими у контрольних тварин.
Інтегральні гематологічні показники у лабораторних тварин при одночасному дослідженні в дозах опа біохімічних та гематологічних показників в обох експериментальних групах тварин не мали суттєвих відмінностей від значень відповідних параметрів у контрольній групі, де замість ліків вводили фізіологічний розчин.
При введенні сольового розчину значних змін з боку досліджуваних органів та ін'єкційного розчину не виявлено.
Патологічних змін у структурі досліджуваних органів та місця ін'єкції не виявлено ні при введенні препаратів тваринного походження в терапевтичних та 10-кратних терапевтичних дозах, ні при фізіологічному розчині.
Основні параметри мікроскопічної будови печінки, нирок, тимусу, селезінки, тканин головного мозку у тварин дослідних груп узгоджувались з показниками щурів контрольної групи.
Для дослідження місцевої подразнюючої дії Супрастину та Супрастину "тваринам вводили препарати суспензії крохмалю крохмально. Оцінку місцевої подразнюючої дії проводили за станом слизової оболонки шлунка. У контрольній групі тварин, як і у групах тварин, які отримували експериментальний препарат та препарат порівняння, виразкові ураження слизової не відзначаються. Одиничні невеликі крововиливи (петехії) спостерігалися у всіх груп лабораторних тварин, їх кількість не залежить від дози препарату.
У групі тварин, які отримували плацебо, g пофарбований і чітко структурований. Судини помірно розширені. У групах лабораторних тварин, які отримували препарат у порівнянні з одноразовою та десятикратною терапевтичною дозою, цитоархітектонічна слизова і підслизова оболонка шлунка не мала явних патологічних змін. Гістологічний малюнок шлунка у серії тварин, які отримували експериментальний препарат, суттєво не відрізнявся від картини у групі контрольних тварин.
Антигістамінний засіб, що відрізняється тим, що виготовляється у формі таблеток і містить як діючу речовину хлоропіраміну гідрохлорид у кількості 10-15% від ваги таблетки, а як допоміжні речовини кукурудзяний крохмаль, амілопектин, тальк, желатин, стеарат магнію і лактози, тоді як масова частка допоміжних речовин від масової частки основної діючої речовини становить:
Кукурудзяний крохмаль і 1,5 - 2,5
Амілопектин - 0,05-0,1
Тальк - 0,2
Желатин - 0,01-0,06
Стеарат магнію - 0,12
Лактоза - відпочинок
- Чи можна пити Супрастин при грудному вигодовуванні
- Альтернативи антигістамінних препаратів
- Чи можу я використовувати Супрастин для немовлят
- Антигістамінні побічні ефекти Коли припинити прийом ліків від алергії; Новини-Медичні
- Чи можна пити Супрастин під час годування груддю