„Розсіюватися за кордоном у суші”: роль дикої природи у розповсюдженні антимікробної стійкості
Кетрін Е. Арнольд
Департамент навколишнього середовища, факультет наук, Йоркський університет, Геслінгтон, Йорк YO10 5NG, Великобританія
Нікола Дж. Вільямс
Департамент епідеміології та здоров'я населення, Інститут інфекції та глобального здоров'я, кампус Ліахерст, Ліверпульський університет, Нестон CH64 7TE, Великобританія
Школа ветеринарної медицини та науки, Ноттінгемський університет, кампус Саттон Бонінгтон, Саттон Бонінгтон, Лестершир LE12 5RD, Великобританія
Кетрін Е. Арнольд
Департамент навколишнього середовища, факультет наук, Йоркський університет, Геслінгтон, Йорк YO10 5NG, Великобританія
Нікола Дж. Вільямс
Департамент епідеміології та здоров'я населення, Інститут інфекції та глобального здоров'я, кампус Ліахерст, Ліверпульський університет, Нестон CH64 7TE, Великобританія
Школа ветеринарної медицини та науки, Ноттінгемський університет, кампус Саттон Бонінгтон, Саттон Бонінгтон, Лестершир LE12 5RD, Великобританія
Анотація
1. Вступ
Зростаюча людська популяція та зростаюча фрагментація природних середовищ існування неминуче змушують живу природу мати більший контакт, як прямий, так і непрямий, з людьми та їх худобою, тим самим збільшуючи можливості передачі інфекції між популяціями та всередині них [1]. Хоча було досягнуто певного прогресу в розумінні епідеміології інфекцій, що спричиняють різноманітні хазяї, що охоплюють дику природу [2], менше уваги приділяється ролі диких тварин в екології та розвитку антимікробної стійкості (АМР) [3,4]. Хоча АМР вважається одним із найбільших викликів глобальній безпеці здоров'я [5], на сьогоднішній день більшість досліджень АМР базуються на клінічних умовах [6]. Відносно мало відомо про потік та долю АМР у природному середовищі [7], особливо у високомобільних видів, які можуть діяти як ефективні диспергатори АМР [3,4] (рис. 1). У цьому огляді ми обговорюємо можливу роль дикої природи у розповсюдженні AMR, зокрема, як дика природа може придбати та транспортувати AMR та потенціал для передачі AMR людям та худобі. 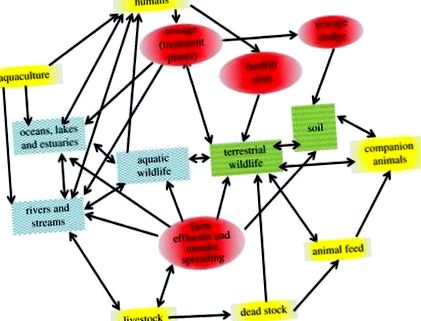
Рисунок 1. Розповсюдження АМР по ландшафту: між людськими громадами, лікарнями, очисними спорудами, фермами та довкіллям, у тому числі за допомогою дикої природи (адаптовано за [6]). (Інтернет-версія у кольорі.)
2. Антимікробна стійкість
Екологія AMR ускладнюється горизонтальним поширенням генів, що кодують AMR, через спільноти різних видів і навіть родів бактерій через мобільні генетичні елементи, такі як плазміди (позахромосомні молекули ДНК). Ці мобільні генетичні елементи часто кодують кілька генів, забезпечуючи стійкість до антимікробних препаратів та, дійсно, інших хімічних факторів, що впливають на навколишнє середовище, включаючи метали та дезінфікуючі засоби. Отже, вплив одного антимікробного препарату (або іншого стресового фактору) може відібрати для всіх кодованих генів і, отже, швидку появу стійкості до різних препаратів [6]. Таким чином, дика природа та інші бактерії навколишнього середовища, яких ніколи не було встановлено, що заражають людей, можуть за допомогою горизонтального перенесення генів обмінюватися механізмами стійкості з патогенами людини [11,12] (але див. [13]).
3. Потенційні джерела протимікробної стійкості навколишнього середовища до дикої природи
Після вибору резистентності серед осіб (людей чи одомашнених тварин), які отримували антимікробні засоби [10], пацієнт виводить як стійкі бактерії, так і антимікробні препарати (рисунок 1). Вони можуть розпорошуватись у навколишньому середовищі, наприклад, у стічних водах, що закачуються у річки [14] та розповсюджуються мули стічних вод як добриво, або у фекаліях обробленої худоби та домашніх тварин [15,16] (рис. 2). Стіки та стіки з полів часто в кінцевому підсумку впадають у море, в результаті чого лимани, прибережні води та пляжі забруднюються фекаліями [14] (рисунок 1). Це може бути критичною точкою контакту, коли люди та морські тварини, а також кулики та морські птахи зазнають впливу АМР [19]. Швидко розростається галузь аквакультури - ще одне джерело AMR та протимікробних речовин для навколишнього середовища: риба та морепродукти, вирощувані в деяких країнах, де вживання антимікробних препаратів є високим і погано регулюється, особливо схильні до перенесення медично значущих стійких патогенів [4,20].
Рисунок 2. Антимікробна стійкість у дикій природі на молочних фермах у Чеширі, Великобританія. Структури опору кишкова паличка з фекалій великої рогатої худоби, гризунів (головним чином Myodes glaroelus і Apodemus sylvaticus), порівнювали диких птахів (переважно вороб’їв) та інших диких ссавців (переважно борсуків та лисиць). (a) Відсоток фекальних зразків, що містять Кишкова паличка стійкий щонайменше до одного антибіотика на шести різних фермах (i – vi). (b) Відсоток Кишкова паличка ізольовані від кожної групи тварин, стійких до різних антибіотиків або стійких до різних препаратів. Випробовували стійкість до таких антибіотиків: ампіцилін (ампер), левоміцетин (хлор), тетрациклін (тет), триметоприм (trm) та налідиксинова кислота (нал), а також MDR (стійкість до декількох препаратів, що визначається як стійкість до трьох або більше випробувані антибіотики). Всі тести на чутливість проводились згідно з рекомендаціями Британського товариства антимікробної хіміотерапії [17]. Детальніше про методи див. У електронному додатковому матеріалі. Малюнок адаптовано за [18]. (Інтернет-версія у кольорі.)
Еволюція AMR не обов’язково зупиняється в шлунково-кишковому тракті тварин (включаючи людей), які перебувають на лікуванні; багато протимікробні засоби можуть виводитися в активній формі та зберігатись у навколишньому середовищі [21]. Таким чином, постійний вплив антимікробних препаратів, наприклад, у стічних водах, може зберегти селективну перевагу АМР та сприяти розповсюдженню детермінантів стійкості та стійких бактерій у навколишньому середовищі. Існує додатковий ризик від місць, сильно забруднених екскрементами, таких як інтенсивні ферми та очисні споруди. Місця з великою кількістю та різноманітністю бактерій забезпечують високу щільність бактеріальних господарів та відмінні умови для горизонтальної передачі генів AMR від коменсальних або навколишніх середовищ до патогенних бактерій [22]. Зрозуміло, що, особливо в районах з густою популяцією людей чи худоби, існує безліч джерел та підсилювачів AMR. Якщо гени та бактерії AMR переносяться в кишечнику дикої природи, а в поєднанні з неадекватним поводженням з відходами та переміщенням тварин на велику відстань, існує можливість для дикої природи транспортувати нові та нові гени AMR по всьому світу [14] (рис.
4. Структури зараження протимікробною інфекцією в дикій природі
Зі збільшенням тиску з боку розширення людської популяції дикі тварини все більше змушені шукати ресурси, забруднені людським «забрудненням патогенами» [2,14]. Тож не дивно, що АМР часто описували у дикій природі, яка перебуває в домашніх умовах [11]. AMR був виявлений, особливо серед бактерій коменсальної кишки, у диких ссавців, птахів, рептилій та риб, причому показники поширеності та стійкості різняться залежно від видів, місцезнаходження та, можливо, часу (наприклад, [3,20,23–27]). Поточні дані про АМР у дикій природі здебільшого складаються із серії «моментальних знімків», що підтверджують наявність резистомів (усіх генів стійкості до антибіотиків, що містяться у мікробів [13]) у цих тварин, але небагато іншого. Однак нечисленні дослідження, які виявляють потенційні джерела AMR і можуть проводити порівняння місць, що відрізняються забрудненням, дають уявлення про можливість дикої природи розповсюджувати клінічно значущі AMR.
Таблиця 1. Антимікробно-стійкий кишкова паличка у фекаліях диких гризунів, зібраних на сайтах у Великобританії, що відрізняються передбачуваним впливом худоби, обробленої антимікробними препаратами. Досліджено стійкість до шести антибіотиків (ампіциліну (ампер), апраміцину (apr), левоміцетину (chl), тетрацикліну (tet), триметоприму (trm) та налідиксової кислоти (nal)) [17]. (N.J.W. & M.B. 2011, неопубліковані дані; [32]). Докладніші відомості див. У електронному додатковому матеріалі.
вид гризунів: водяна полівка, Арвікола амфібія; польова полівка, Microtus agrestis; банківська полівка, Myodes glareolus; деревна миша, Apodemus sylvaticus; домашня миша, Mus musculus.
b Водяні полівки на цих островах є скоріше фосирними, ніж прибережними, як на материку.
c Захоплений у будинках птиці та навколо них.
Отже, в той час як більшість досліджень в дикій природі припускають, що АМР у дикій природі є наслідком поширення стійких бактерій від домашніх тварин чи людей [33,34], існує кілька невиключних альтернативних гіпотез, які оскаржують це поняття недавньої передачі. Наприклад, після впливу відходів, що містять фармацевтичні препарати, кишкові бактерії, присутні в дикій природі, розвивають стійкість завдяки відбору вже існуючих екологічних генів AMR. Вони можуть «натуралізуватися» в мікробіоти кишечника, але також гени AMR (які були знайдені в древніх зразках навколишнього середовища [13]) є і завжди були нормальною знахідкою в мікробіотах коменсальної кишки. Більше того, розрізнити АМР, нещодавно придбану від антропогенних джерел, таких як ферми чи очисні споруди, та „внутрішню” (або, принаймні, „натуралізовану”) ПМР буде складним завданням. Порівняння подібності послідовностей генів стійкості, зібраних із сайтів, що відрізняються своєю зв'язком, із джерелами набутих AMR (наприклад, з використанням підходів до мережі подібності послідовностей [12]) може надати необхідні докази.
5. Вивчення розповсюдження протимікробної стійкості дикими тваринами
З огляду на численні прогалини в знаннях, буде необхідний ряд інструментів та підходів для виявлення та характеристики шляхів передачі АМР у дикій природі. У широкому масштабі ідентифікація ознак, які схильні до видів диких тварин або функціональних груп для передачі АМР, може бути визначена шляхом інтеграції наборів екологічних, біологічних та життєвих історій для хребетних господарів з метагеномними послідовностями, що включають детермінанти стійкості [12]. Хоча це ефективний та інформативний підхід, одне застереження полягає в тому, що, видобуваючи такі дані, ми можемо знайти лише відомі детермінанти опору. Деякі дані досліджень дикої природи показують, що гени, відповідальні за фенотипову стійкість, часто неможливо виявити за допомогою ПЛР (ланцюгових реакцій полімерази), спрямованих на загальні клінічні гени AMR. Це свідчить про більшу різноманітність генів стійкості (багато з яких вже були пов’язані з іншими функціями, не пов’язаними з AMR) у навколишньому середовищі, ніж у клінічних ізолятах (K.E.A., N.J.W. та M.B. 2011, неопубліковані дані).
У більш точному масштабі необхідні навчальні системи, в яких існують чіткі та вимірювані шляхи передачі АМР та можна відстежувати пересування дикої природи. Виявлення стійкості до різних препаратів у видів, що мають високу природоохоронну цінність на океанічних островах [25], та у зразках із ізольованих, відносно недоторканих точок на континентах [27] забезпечують "природні експерименти", які ідеально підходять для вивчення закономірностей та процесів в екології та еволюція AMR. Моніторинг генів AMR у таких незайманих екосистемах (наприклад, в Арктиці чи природних заповідниках з жорсткою біозахистом) або на їх межі з територіями, що знаходяться під впливом людини, дозволяє нам оцінити частоту обміну генами, що кодують опір, у мікробних спільнотах. Такі мікробні спільноти можуть існувати в популяціях людей, домашніх тварин та дикої природи, а також у ширшому середовищі [27,37].
6. Наслідки протимікробної стійкості для дикої природи
Наслідки для дикої природи еволюції AMR у коменсальних або навіть патогенних бактеріях не перевірені [37], але, ймовірно, невеликі. Наприклад, на відміну від пташиного грипу [41], АМР не є хворобою і, здається, не зменшує виживаність або здатність до розповсюдження «заражених» тварин, хоча це не було явно перевірено. Клінічна проблема з АМР як серед людей, так і серед поголів'я худоби полягає не в тому, що він викликає захворювання, а в тому, що він загрожує здатності лікувати інфекції антимікробними препаратами, що рідко зустрічається у диких популяцій. AMR може скомпрометувати лікування окремих диких тварин у неволі, наприклад у лікарнях дикої природи або в групах з високим рівнем управління, особливо тих, що страждають від імунітету через низьке генетичне різноманіття (наприклад, [42]). Це може посилитися завдяки заходам управління охороною, таким як транслокація рідкісних видів, які можуть пришвидшити поширення нових мікробів або антимікробних генів між ізольованими популяціями [43].
Найбільшою проблемою для популяцій дикої природи є реакція керівництва, якщо вони вважаються важливими джерелами AMR для людей або худоби (див. Також таблицю 2). Боротьба з інфекціями дикої природи, що передаються людям та худобі, ґрунтується на трьох основних підходах - поділ або, принаймні, зменшення контакту з джерелом дикої природи, вакцинація та контроль популяції дикої природи, часто шляхом вибракування. Вакцинація неможлива для боротьби з АМР, а фізичне відокремлення дикої природи від худоби є складним, дорогим і, за винятком дуже локального (наприклад, утримання гризунів або птахів поза сховищами кормів), неможливим. Захист харчового ланцюга людини від АМР є важливим, але складним завданням, враховуючи, що дика дичина, морепродукти та м'ясо куща є важливими як у харчовому, так і в культурному відношенні для багатьох людських суспільств [4]. Крім того, заходи контролю та пом'якшення, такі як поліпшення гігієни та обмеження пересування, не можуть бути легко вжиті, якщо взагалі, для вільноживучих тварин. З логістичних, економічних, історичних та культурних причин вибракування часто застосовується: однак, ефективність та ефективність вибракування диких тварин у боротьбі з хворобами в кращому випадку суперечливі.
Таблиця 2. Короткий зміст деяких ключових невирішених питань, заходів щодо пом'якшення наслідків та дослідницьких підходів щодо ролі дикої природи у передачі АМР на основі проведеної літератури. Запропоновані дослідницькі підходи спираються на різні дисципліни, включаючи екологію, ветеринарію та соціальні науки.
7. Дослідження та пріоритети політики
Дика природа явно линяє і, отже, здатна поширювати AMR [2,4]. Однак мало досліджень виявили ймовірні фактори відбору (включаючи, але не обов'язково, джерела антимікробного впливу), походження генів стійкості або, що важливо, напрямок передачі. Вивчення передачі інфекції в дикій природі створює низку проблем, особливо для такого складного питання, як AMR, який присутній і може переміщатися між множинними бактеріальними таксонами у багатьох господарів та навколишнього середовища. Підходи, що використовуються для вивчення та контролю передачі АМР у клінічних умовах, є складним завданням для застосування в системах дикої природи. Контакт між дикою природою та джерелами АМР та/або антимікробними препаратами часто неможливо виміряти безпосередньо, однак потрібно робити висновки, наприклад, з молекулярних «відбитків пальців» конкретного забруднення. Це можна доповнити поведінковими спостереженнями та електронними приладами для відстеження, встановленими для диких тварин.
Втручання, що мінімізує та пом'якшує передачу АМР від поголів'я худоби чи людства до дикої природи, потребує досліджень поряд із дослідженням самого ризику, щоб розробити як науково обгрунтовані, так і пропорційні протоколи та політику (таблиця 2). Контроль за забрудненням та очищення стічних вод є, ймовірно, пріоритетними напрямами таких досліджень, особливо в країнах, де мало контролюється як вживання антибіотиків, так і викид необроблених відходів (що включає як розвинені, так і країни, що розвиваються). Тим часом для збору зразків для спостереження можуть бути набрані екологи, які вивчають популяції диких тварин, а також лікарні для диких тварин та існуючі програми, призначені для моніторингу забруднення, отруєнь та хвороб у дикій природі (наприклад, WILDCOMS [44]). Цей останній підхід може бути особливо корисним для виявлення видів, ключових особин у популяціях або просторових місцях, які є «суперпоширеними» передавачами АМР і можуть бути націлені на цілеспрямовані наглядові, контрольні або пом'якшувальні заходи [40].
Важливо вивчити АМР у дикій природі як потенційну небезпеку для здоров'я людей та продовольчої безпеки, особливо з огляду на те, що, як вважають, близько 40% нових захворювань людей походять з дикої природи [1]. Тропічні екосистеми та райони, в яких люди живуть поблизу худоби та дикої природи, можуть представляти підвищений, але на сьогоднішній день недостатньо вивчений ризик для еволюції та передачі АМР з боку дикої природи (таблиця 2). Крім того, дослідження АМР у дикій природі можуть мати більший вплив, ніж просто ризик для громадського здоров'я. По-перше, вийшовши за межі «гри звинувачення» тваринництва, ветеринарної та медичної систем, вони можуть висвітлити фундаментальні проблеми еволюції та екології передачі антимікробно-стійких бактерій та детермінанти стійкості, які можуть бути застосовані в більш клінічних умовах. По-друге, краще розуміння ролі дикої природи у розповсюдженні АМР має допомогти нам вирішити, чи потрібні стратегії контролю та пом'якшення наслідків та де найкраще їх застосовувати. Нарешті, хоча дика природа може бути розповсюджувачем АМР на великі відстані, вона також може бути сторожем за чисельність та розповсюдження забруднення патогенами в нашому середовищі.
Етика
Усі проведені роботи відповідали законодавчим вимогам країни, в якій проводилась робота, та всім інституційним вимогам.
Внески авторів
Усі автори сприяли написанню цього огляду та дали остаточне схвалення для публікації.
- Естрадіол Нові докази захисної ролі проти інсулінорезистентності та ожиріння
- Кордони, що переглядають роль контрзахисту щодо вправ щодо регулювання енергетичного балансу під час
- Годування лапок дикої природи
- Frontiers Роль дієти, харчової поведінки та втручання в дієту в сезонний афективний
- Глікемічний індекс, глікемічне навантаження та волокно відіграють роль у чутливості до інсуліну, індексі диспозиції,