Пацієнтів після гастректомії потрібно спостерігати протягом 20-30 років
Листування: Frank I. Tovey, 5 Crossborough Hill, Basingst oke RG21 4AG, Великобританія
Телефон: 01256-461521 Факс: 01256-323696
Анотація
ЦІЛЬ: Дослідити частоту та лікування харчових дефіцитів після гастректомії.
МЕТОДИ: Популяція гастректомії з 227 пацієнтів у Лондоні спостерігалася протягом 30 років після операції з метою виявлення та лікування харчових дефіцитів.
РЕЗУЛЬТАТИ: На кінець першого десятиліття дефіцит заліза був найпоширенішою проблемою. Дефіцит вітаміну В12 став більш важливим у другому десятилітті. Протягом третього десятиліття вони досягли однакової поширеності, виявившись приблизно у 90% жіночого та 70% чоловічого залишкового населення. Дефіцит вітаміну D був меншою проблемою, досягнувши апогею у другому десятилітті. Загалом у всіх жінок було гірше, ніж у чоловіків.
ВИСНОВОК: Підкреслюється важливість довгострокового спостереження за недостатністю шлунково-кишкового тракту за дефіроном форірону, вітаміну В12 та вітаміну D.
ВСТУП
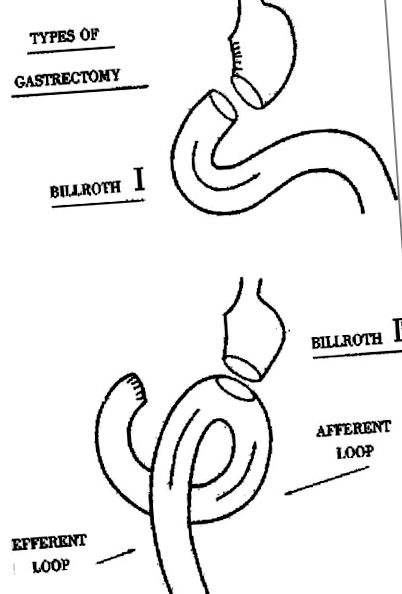
У 1981 та 1984 роках, завдяки люб'язності Китайської академії медичних наук, перший автор відвідав центри на півночі та півдні Китаю, щоб зібрати інформацію про поширеність виразки дванадцятипалої кишки та її зв'язок із основними дієтами. Було зазначено, що стандартною операцією при виразці дванадцятипалої кишки у багатьох центрах була або резекція шлунка Billroth II (шлунково-кишковий тракт), або Billroth I (гастродуоденальний анастозний омоз) (рис. (Рис. 1). 1). Це підвищує ймовірність того, що в даний час в Китаї може існувати популяція гастректомії у віці 25-30 років, яка, можливо, розвинула харчові розлади в результаті їх роботи. Наш досвід дослідження пацієнтів через 25-30 років після шлунково-кишкового тракту та на вестерновій дієті може слугувати орієнтиром щодо частоти цих проблем.
Види шлунково-кишкового тракту.
МАТЕРІАЛИ І МЕТОДИ
Пацієнти
Ми повідомляємо результати лонгитюдного дослідження у Великобританії. Дослідження було проведено в лікарні Університетського коледжу в Лондоні на пацієнтах, які перенесли резекцію шлунка між 1955 і 1960 рр. [1]. У 1969 р. Було встановлено контакт з 227 пацієнтами, і хоча кількість зменшилася внаслідок переїзду в інше місце або смертності, за рештою спостерігались регулярно до 1990 р. Населення включало 186 пацієнтів, які перенесли гастректомію Білльта II (чоловіки 141, жінки 45) і 41 які перенесли резекцію шлунка за Біллротом I (чоловік 24, жінка 17). Через інтервал 10–15 років після операції їх щорічно перевіряли або частіше, якщо це було вказано, і проводили наступні дослідження, щоб виявити можливі порушення харчування [1].
Метод
Клінічне дослідження (при першому відвідуванні) Пацієнтів зважили. Порівняно з ідеальною передопераційною вагою пацієнта, втрата до 4,5 кг розцінювалася як помірна втрата, а більша втрата як важка.
Було зафіксовано будь-які постпрандіальні симптоми, включаючи зменшену продовольчу здатність, достроковий демпінг та пізній демпінг. Помірно знижена дієздатність розглядалася як можливість приймати половину того, що пацієнт зазвичай сподівався з’їсти під час їжі, а важка - на третину або менше. Було записано тих, хто зі зниженою ємністю виявляв дискомфорт або блювоту, якщо кількість була перевищена. Ранні демпінги складалися із слабкості, непритомності, пітливості та серцебиття через 10-20 хв після їжі. У тих, хто пізно відмовився, подібні симптоми виникали приблизно через 30-60 хв після закінчення їжі.
Постійну діарею характеризували як помірну, якщо спостерігалося до 3 рідких стільців на день, і як важку, якщо більше. Всі 9 пацієнтів з діареєю мали 24-годинні оцінки жиру у фекаліях, а також стільки ж інших пацієнтів, які бажали (загалом 158). Вихід жиру з калу 6 г/добу-12 г/добу розцінювали як помірну стеаторею та вище 12 г/добу як важку.
Нестачі харчування
Дефіцит заліза Повний аналіз крові включає картину крові, залізо в сироватці крові та загальну здатність зв’язувати залізо (TIBC). Дефіцит заліза визначався як насиченість залізом (сироваткове залізо/загальна здатність до зв’язування заліза) нижче 16%.
Дефіцит вітаміну В12 Дефіцит вітаміну В12 діагностували, коли два розділені біопроби, повторені через один місяць, показали значення менше 110 пмоль/л.
Дефіцит вітаміну D Кальцій, фосфат і лужна фосфатаза в сироватці крові. Першою ознакою було підвищення оцінки рівня лужної фосфатази в сироватці крові. Якщо це було встановлено, проводились тести функції печінки для виключення печінкової причини. Інші причини, такі як хвороба Педжета, нещодавні переломи або кісткові вторинні захворювання були виключені. Вихід кальцію у сечі протягом 2 годин нижче 2 ммоль/24 год підтверджував діагноз [2]. Потім було проведено терапевтичне дослідження кальцію та вітаміну D як діагностичний захід, а стійке падіння рівня лужної фосфатази в сироватці крові підтвердило діагноз. Таблетки кальцію та вітаміну D BPC лактат кальцію 300 мг, фосфат кальцію 150 мг, кальциферол 12,5 мкг) вводили у дозі 2 таблетки 4 рази на день і дозу зменшували до 2 таблеток 3 рази на день, коли рівень лужної фосфатази в сироватці крові впав до норми.
Остеопороз До 1989 року була проведена рентгенографія правої другої п'ясткової кістки та вимірювання, зроблені на рентгені другої правої п'ясткової кістки, ми використовували для обчислення індексу Екстона-Сміта:
де Т - товщина кістки, М - медулярна товщина в середині точки, а L - загальна довжина [3].
Після 1989 року стала доступною рентгенівська абсорбціометрія з подвійною енергією (DEXA), яка використовувалася для скринінгу решти населення. Вибирали лише чоловіків, оскільки до того часу всі пацієнтки були в постменопаузі, що вводило ще один потенційний фактор для остеопоротичних змін.
Статистика Статистичний аналіз проводили із використанням критерію Стьюдента або точного критерію Фішера, якщо це необхідно.
РЕЗУЛЬТАТИ
Клінічні дані
Під час першої подальшої консультації в цьому дослідженні 66 (29%) з 227 пацієнтів мали помірну та 15 (7%) важку втрату ваги. 107 (47%) пацієнтів скаржиться на зниження дієздатності, яка була важкою у 41 (18%)
Ранній демпінг був діагностований у 39 (17%), а пізній демпінг - у 7 (3%). Постійна діарея спостерігалася у 9 із 186 пацієнтів Billroth II (важка у 1), але ні в одного з 41 з гастректомією Billroth I. Різниця не була суттєвою (точний тест Фішера P = 0,2089). П'ятеро з цих 9 пацієнтів мали середню та 2 важкі форми стеатореї.
Помірна стеаторея виявлена після обох операцій [Billroth I, 9 (24%) з 37; Білрот II, 14 (12%) із 121; незначне, P = 0,2292].
Дефіцит вітаміну В12 У більшості пацієнтів падіння концентрації В12 у сироватці передувало будь-якому макроцитозу, зсуву нейтрофілів або анемії. Пацієнтів лікували внутрішньом’язовими ін’єкціями 1000 мкг гідроксокобаламіну в різні місяці. Поширеність серед решти населення показана в таблиці Таблиця1. 1. Можна помітити, що дефіцит заліза стався набагато раніше, ніж дефіцит В12, який з’явився у багатьох пацієнтів протягом перших 10 років після операції. Дефіцит вітаміну В12 розвивався здебільшого через 10-20 років після операції, і його поширеність повільно зростала до рівня дефіциту заліза до кінця 25-30 років, коли приблизно у 70% чоловіків та 90% жінок розвивався дефіцит заліза або В12, недоліки поєднуються відповідно в 51% та 70%.
Дефіцит вітаміну D Дефіцит вітаміну D спостерігався у 7,5% шлунково-кишкового тракту Billroth II та 7,3% Gastroctomі Billroth I, і це була переважно проблема жінок. (F: M = 19%: 4%). Це стало очевидним у багатьох пацієнтів протягом перших 10 років після операції (табл. (Табл. 1). 1). З досліджених 50% мали тяжку та 28% помірну стеаторею порівняно з 20% та 14% відповідно для всієї серії.
Остеопороз Остеопоротичні зміни, що перевищують нормальне старіння, ми спостерігали у 24%, 20% та 22% чоловіків та у 35%, 51% та 86% жінок у 1969, 1974 та 1982 роках, відповідно. Жоден з них не мав доказів дефіциту вітаміну D. Однак ці вимірювання були недостатньо чутливими для моніторингу будь-якого лікування протягом короткого періоду [4].
Подвійну енергетичну рентгенівську абсорбціометрію застосовували у 16 активних пацієнтів чоловічої статі, без ознак дефіциту вітаміну D, які все ще відвідували клініку. У шести (37,5%) було виявлено зниження мінеральної щільності кісток поперекового відділу хребта та верхньої лівої стегнової кістки більш ніж на 2 стандартних відхилення. Спочатку їх лікували добавкою кальцію (мікрокристалічний гідроксиапатит) 16 г/добу-32 г/добу та кальциферолом по 0,25 мг на день, але без відповіді. Після цього їм давали періодичний циклічний етидронат по 400 мг щоночі протягом 2 тижнів, потім карбонат кальцію, еквівалентний 500 мг кальцію щодня протягом 10 тижнів. Цей 12-тижневий цикл повторювався протягом 2 років. Лише 2 пацієнти відповіли, повернувшись до норми значень. На сьогоднішній день не було зареєстровано повністю задовільного лікувального лікування постгастректомічного остеопорозу [5].
ОБГОВОРЕННЯ
Кілька факторів [6-11] сприяють харчовим розладам після гастректомії. При втраті пілоричного сфінктера відбувається неконтрольоване спорожнення шлунка, і здатність до їжі стає залежною від здатності тонкої кишки вміщувати їжу. Швидке спорожнення стимулює перистальтику, і відбувається швидке проходження їжі через тонкий кишечник. Невеликі молекули, такі як цукри та крохмалі, які швидко розщеплюються в малих кишечниках, виробляють сильний осмотичний ефект, що призводить до втягування в кишечник позаклітинної рідини на 2-3 літри, що призводить до падіння обсягу плазми та підвищення гематокриту. Це потрапляння рідини розширює кишечник, і може спостерігатися раннє насичення та зниження здатності до їжі. Коли падіння обсягу плазми перевищує 7%, у деяких пацієнтів розвивається ранній демпінг із гіпотонією відповідно до їх судинної толерантності (рис. У інших пацієнтів швидке всмоктування глюкози з кишечника призводить до надмірної секреції інсуліну з подальшою гіпоглікемією та симптомами пізнього демпінгу.
Підвищений вміст води в матеріалі, що потрапляє в товстий кишечник, може спричинити діарею, якщо товста кишка не здатна поглинати рідину. Наявність неперетравлених цукрів та крохмалю також може діяти як подразник. Швидке проходження їжі через тонкий кишечник призводить до зменшення змішування з ферментами підшлункової залози та кишечника. Це призводить до порушення травлення та всмоктування білків та жирів, як свідчить наявність стеатореї у деяких пацієнтів. Коротке замикання дванадцятипалої кишки під час операції Білльта II (рис. (Рис. 1) 1) може спричинити відставання соків підшлункової залози від їжі, що виявляється наявністю важкої стеатореї в цій групі.
Поглинання вітаміну D залежить від розчинності жиру, а поєднання стеатореї та зменшення споживання вітаміну D може призвести до дефіциту вітаміну D. Як вже згадувалося, у багатьох пацієнтів, особливо у жінок, виникає селективна огида до певної їжі, особливо до джерел вітаміну D: це пояснювало б збільшення частоти дефіциту вітаміну D у цій групі.
Обмін заліза також може бути порушений. Вживання залізовмісних продуктів може бути зменшено. Значна частина споживання відбувається у вигляді заліза із заліза або заліза в поєднанні з білком. Кислота потрібна для перетворення заліза із заліза у залізне, кислота та пепсин - для перетворення органічного заліза в неорганічне. Як шлунково-кишковий тракт, так і кислота та пепсин знижуються. Крім того, велика частина заліза всмоктується в дванадцятипалій кишці і верхній частині товстої кишки.
Також може розвинутися дефіцит вітаміну В12. Одним із факторів є втрата внутрішнього фактора, який секретувався слизовою оболонкою шлунка, видаленою шлунково-кишковою магістраллю. Швидке проходження через тонкий кишечник призводить до меншого всмоктування.
Всмоктування кальцію також відбувається головним чином у дванадцятипалій кишці та верхній частині товстої кишки, і це погіршується кишковою спешкою та втратою неперервності дванадцятипалої кишки. Крім того, якщо присутня стеаторея, всмоктування кальцію ще більше погіршується утворенням нерозчинного мила кальцію.
В результаті всіх цих факторів у пацієнтів після гастректомії може розвинутися залізодефіцитна анемія, дефіцитна анемія вітаміну В12, дефіцит вітаміну D та остеомаляція, або остеопороз, що перевищує нормальне старіння.
Висновок Це дослідження, зокрема, демонструє зростаючу поширеність дефіциту заліза та вітаміну В12 у популяції після газової тректомії, яка досягає приблизно 75% за 20-30 років. Це наголошує на зростаючому значенні з роками регулярного моніторингу насичення заліза та рівня В12. Крім того, підвищений рівень лужної фосфатази в сироватці може свідчити про дефіцит вітаміну D і потребує дослідження. Зараз, коли резекція шлунка рідко виконується при виразковій хворобі, важливо пам’ятати, що існує велика кількість пацієнтів, які перенесли шлунково-кишкового тракту 20-30 років тому, і у них виникає ризик розвитку харчових дефіцитів.
ПОДЯКИ
Автори хочуть подякувати Медичному часопису Pos-tragduate за дозвіл на відтворення даних із "Популяції шлунково-кишкового тракту: 25-30 років" 1990; 66: 450-456
- Пацієнти з високим ризиком розвитку коронавірусу повинні стежити за цим загальним захворюванням печінки, лікар
- Пацієнти зі складними фіброаденомами можуть уникати хірургічного втручання, рекомендації щодо дослідження - ScienceDaily
- Пацієнтам слід запитати хірургів про використання меду для загоєння ран - ScienceDaily
- Пацієнти з гіпертонічною нефропатією та хронічною хворобою нирок можуть не отримати сувору користь
- Підвищення рівня ожиріння підкреслює потребу в посиленому догляді; Постгострі моделі перехідного догляду