Реакції інтерлейкіну-15 на атрофію скелетних м’язів, спричинену старінням та розвантаженням
Анотація
інтерлейкін - 15 (IL-15) - нещодавно виявлений цитокін (20), який належить до чотирьох сімейств пучків α-спіралі цитокінів, які також включають IL-2, IL-3, IL-4, IL-5, IL- 6, ІЛ-7 та ІЛ-9. Показано, що ролі IL-15 в імунній системі включають проліферацію та виживання CD8 + Т-клітин (6), активацію природних клітин-кілерів (11) та проліферацію В-клітин (5). МРНК IL-15 також конститутивно експресується в широкому діапазоні типів клітин і тканин, включаючи плаценту, скелетні м'язи, печінку, епітеліальні клітини та активовані макрофаги (20).
IL-15 та IL-2 виконують надлишкові ролі, що є результатом подібного рецепторного складу для цих двох цитокінів. Рецептори IL-15 та IL-2 (IL-15R, IL-2R відповідно) - це тримерні структури, що складаються з двох однакових ланцюгів, β-ланцюга IL-2R/IL-15R (IL-2Rβ) та загального γ ( γc) -ланцюг, поряд із конкретними α-ланцюгами (18). IL-15Rα виявляє високу спорідненість до білка IL-15 з а Кd 10 pM (14). На додаток до паракринних дій, IL-15 може експресуватися в транс, в якому цитокін або пов'язаний з клітинною поверхнею IL-15Rα, або прикріплений до клітинної мембрани. Таким чином, зрілий IL-15 може бути представлений сусіднім клітинам, які експресують IL-2Rβ і -γc (7). Хоча і мРНК IL-15 (27), і IL-15Rα (19) експресуються в скелетних м'язах, невідомо, чи мРНК для функціонального тримерного IL-15R також експресується в скелетних м'язах, що дозволило б переклад презентація IL-15 м’язовими клітинами.
Всередині скелетних м’язів IL-15 може стимулювати експресію білка важкої ланцюга міозину в диференційованих міотрубках (17, 34). Міотрубки, культивовані IL-15, також мають гіпертрофічну морфологію у порівнянні з контрольними культурами, які не містять IL-15. Крім того, було показано, щоденні ін’єкції білка IL-15 зменшують фрагментацію ДНК м’язів шлунково-кишкового тракту, послаблюють втрату скелетних м’язів, пов’язану з раком (кахексія), і зменшують експресію генів рецептора фактора некрозу пухлини типу I (TNFR) у моделі раку на гризунах (15). Хоча ці результати демонструють позитивний ефект екзогенного білка IL-15 у міоцитах, відповідь ендогенного внутрішньом'язового IL-15 не досліджували. Крім того, реакція IL-15 на втрату м'язів, яка виникає внаслідок таких станів, як старіння або розвантаження м'язів, невідома.
Усі експериментальні процедури були схвалені Інституційним комітетом з догляду та використання тварин від Медичної школи Університету Західної Вірджинії. Відповідно до стандартів догляду за тваринами було дотримано рекомендацій щодо догляду за лабораторними тваринами, які пропагує Американська асоціація з акредитації лабораторних доглядів за тваринами, і дотримуючись політики та процедур, деталізованих у Посібник з догляду та використання лабораторних тварин як опубліковано Департаментом охорони здоров'я та соціальних служб США та проголошено в Законі про захист тварин.
Гризун HS.
Навантаження/розвантаження крила.
RT-PCR оцінки мРНК.
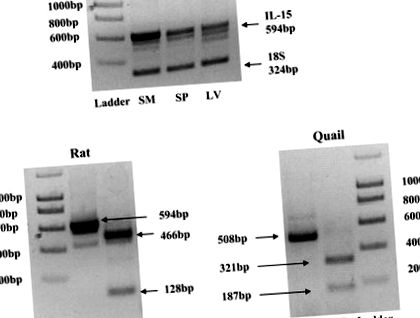
Рис. 1.Специфічність праймера до інтерлейкіну (IL) -15. В: RT-PCR проводили для IL-15 в кДНК скелетних м'язів щурів (SM), з кДНК тканини селезінки (SP) та тканини печінки (LV), що використовувались як позитивний контроль. Тридцять чотири цикли ПЛР при розрахунковій температурі відпалу (TA) 56,6 ° C давали смуги 594 bp у всіх трьох типах тканин. B: обмеження перетравлення продуктів ПЛР IL-15 із скелетних м'язів щурів та перепілок АлуI рестрикційний фермент. Інкубація продуктів ПЛР при 37 ° С протягом 1 год утворювала передбачувані фрагменти. ПЛР, повний ПЛР-продукт; RD, продукти, що засвоюються ферментом рестрикції, ПЛР.
Таблиця 1. Інформація про ПЛР-праймер
ТА, температура відпалу; ІЛ, інтерлейкін; R, рецептор; γc, загальний γ; F, вперед; R, реверс.
Секвенування IL-15Rα.
ПЛР-ампліфікація послідовності ратусу IL-15Rα дала продукт ПЛР на 100 п.н. більший, ніж очікувалося. Відповідні продукти ПЛР очищали гелем за допомогою комерційно доступного набору для екстракції гелю відповідно до інструкцій виробника (QIAquick Gel Extraction Kit; Qiagen Sciences) та направляли на пряме секвенування (SeqWright DNA Technology Services, Houston, TX). Потім нещодавно отриману інформацію про послідовності кДНК порівнювали з передбаченою комп'ютером послідовністю, спочатку використаною для проектування праймерів ПЛР (XM_577598).
Статистичний аналіз.
Статистичний аналіз проводили за допомогою програмного пакету SPSS, версія 10.0. Дані аналізували за допомогою 2 × 2 ANOVA для вивчення основних ефектів старіння та розвантаження та взаємодії віку × розвантаження. Дані представлені як середнє значення ± SE з значенням, встановленим на P
Таблиця 2. Характеристика м’язів гризунів
Значення - середні значення ± SE; n, ні. тварин. HS, підвіска задньої кінцівки; BM, маса тіла. Характеристика 20 молодих дорослих (5–7 міс.) Та 18 стареючих (33 міс.) Самців щурів Fischer 344 × коричневих норвезьких щурів. NS, не значуще.
* P
Рис.2.Зміни транскрипції IL-15 після суспензії задніх кінцівок (HS). A: Експресія мРНК IL-15 у м’язах підошви після HS. B: Експресія мРНК IL-15 у м’язах підошви після HS. Значне взаємодія старіння × розвантаження спостерігалося в обох скелетних м’язах, вказуючи на те, що вік впливав на реакцію мРНК IL-15. Дані виражаються як середні значення ± SE з значенням на P
У будь-якій точці часу в моделі перепелів не було значної взаємодії старіння × навантаження/розвантаження. Тим не менше, спостерігався значний основний ефект старіння, і мРНК ІЛ-15 була на 53% більшою у вікових м'язах ПАТ порівняно з м'язами молодих дорослих птахів. Цей основний вплив віку на експресію IL-15 був значущим для всіх станів: 14 днів перевантаження (F = 5,8, P = 0,024), 7 днів розвантаження (F = 97,8, P
Рис.3.Зміни транскрипції IL-15 у відповідь на перевантаження крила та подальше розвантаження. Експресія мРНК ІЛ-15 у м'язах патагіалісу після 14 днів перенапруження, 14 днів навантаження з наступним 7 днів наступного розвантаження та 14 днів навантаження з наступним 14 днів розвантаження. Дані виражаються як середнє значення ± SE з значенням, встановленим на P
Секвенування рат IL-15Rα.
Комп'ютерно передбачена послідовність мРНК від GeneBank для ланцюга rattus IL-15Rα була використана для побудови праймерів ПЛР (XM_577598). Продукт ПЛР мав прогнозований розмір 325 п.н. після посилення. Однак після ПЛР-ампліфікації та подальшого гель-електрофорезу продукт ПЛР був ближчим до 400 п.н., не спостерігаючи множинних смуг (рис. 4A). Продукт ПЛР очищали гелем, секвенували і порівнювали з передбаченою комп'ютером послідовністю від GeneBank. Нова секвенированная кДНК була ідентичною прогнозованій послідовності на 5′- і 3′-кінцях, з унікальною послідовністю з 103 основ, що містяться в середині (рис. 4B). Після перевірки шляхом секвенування ДНК та обмеження перетравлення з ЗадніIII (рис.4A), нова послідовність була подана до GeneBank (номер приєднання: DQ157696).
Рис.4.Унікальна послідовність α рецептора IL-15 (IL-15Rα) в скелетних м’язах ратусів. A: репрезентативне гелеве зображення IL-15Rα після ПЛР-ампліфікації та рестрикційного перетравлення ХіндIII. Інкубація продуктів ПЛР при 37 ° С протягом 1 год давала передбачувані фрагменти 260 та 131 п.н. ЗадніСайт рестрикції III був унікальним для нової послідовності IL-15Rα, DQ157696. B: порівняння послідовностей раттусу IL-15Rα після послідовності ДНК. Інформацію про нову послідовність порівнювали з передбаченою комп'ютером послідовністю мРНК (XM_577598). Обидві послідовності були ідентичними на 5'- і 3'-кінцях, але нова секвенированная кДНК містила 103 унікальних підстави.
Експресія IL-15R в скелетних м'язах.
Праймери, специфічні для трьох ланцюгів IL-15R (α, β та γ) та ланцюга IL-2Rα, були сконструйовані для вивчення експресії мРНК у скелетних м’язах щурів. МРНК, виділену з тканини селезінки гризунів, використовували як позитивний контроль для кожного з цих праймерів (рис. 5A). Як показано на рис. 5B, Скелетні м’язи щурів експресують мРНК для кожного з ланцюгів IL-15R. Крім того, в селезінці та скелетних м’язах була виявлена мРНК для IL-2R-специфічного α-ланцюга.
Рис.5.Експресія мРНК тримера IL-15R в скелетних м'язах. A: як позитивний контроль, ПЛР-ампліфікацію окремих компонентів IL-15R та IL-2R проводили в кДНК, виробленій з тканини селезінки, і порівнювали з реакціями ПЛР, що проводились в кДНК скелетних м’язів. Обидві селезінки (A) та скелетних м'язів (B) тканина містила мРНК для всіх компонентів IL-15R та IL-2R.
ІЛ-15 і скелетних м’язів.
Перша доповідь про вплив IL-15 на скелетну мускулатуру продемонструвала його здатність збільшувати вміст білка важкої ланцюга міозину в диференційованих миотрубках C2C12 миші in vitro (34). Згодом ці результати підтвердили дані у первинних культурах клітин скелетних м’язів людини (17). Цей ефект IL-15 не залежав від гіпертрофічних ефектів інсуліноподібного фактора росту-I (33), що може стати важливим із старінням, коли рівень анаболічних гормонів зазвичай знижується (40). У цьому дослідженні мРНК IL-15 була більшою у всіх обстежених вікових скелетних м'язах і, як правило, зростала в результаті розвантаження. Ми вважаємо, що це вікова адаптація скелетних м’язів для протидії втраті м’язів у відповідь на атрофічні подразники. Подальші дослідження повинні розглядати ефективність ІЛ-15 для збереження м’язової маси у вікових тварин та у відповідь на умови, що сприяють атрофії м’язів.
ІЛ-15 та апоптоз.
Про роль IL-15 у послабленні апоптозу пропонують дані, що показують, що екзогенний білок IL-15 інгібує апоптотичну сигналізацію, пов'язану зі шляхами смерті. Багатосистемний апоптоз, ініційований у мишей шляхом лікування анти-Fas антитілом, придушувався ін’єкцією тривалого злитого білка IL-15-IgG2b (9). Крім того, трансгенні миші IL-15 стійкі до летальної дози кишкова паличка (23). Введення ІЛ-15 контрольним мишам також знижує рівень смертності від летальної атаки Кишкова паличка. Далі дані показують, що введення IL-15 ізольованим клітинам очеревини in vitro запобігало індукованому TNF-α апоптозу (23).
Добре охарактеризований шлях загибелі клітин, ініційований зв'язуванням TNF-α із TNFR типу I (тобто зовнішнім апоптотичним шляхом), може бути змінений із збільшенням білка IL-15. Наприклад, щоденні ін'єкції білка IL-15 протягом 7 днів у моделі раку на гризунах призвели до значного зниження експресії генів як TNFR типу I, так і типу II (15). Крім того, інкубація фібробластів з IL-15 in vitro послаблює апоптоз, індукований TNF-α (8). Апоптотичний шлях TNF-α був порушений, коли цитоплазматична сигнальна молекула TRAF2, яка зазвичай опосередковує апоптотичний сигнал від TNFR, була завербована на цитоплазматичну сторону IL-15Rα. Цікаво, що такий набір TRAF2 до IL-15Rα спостерігався лише тоді, коли як TNF-α, так і білок IL-15 були присутні в культуральних середовищах (8). Таким чином, IL-15, здається, функціонує, принаймні частково, інгібуючи апоптоз, блокуючи передачу сигналів за течією TNFR. Це актуально для старіючих м'язів, оскільки зовнішній апоптотичний шлях є дуже активним у вікових скелетних м'язах (31). Ми припускаємо, що зміни в мРНК IL-15, які спостерігаються в цьому дослідженні, можуть представляти спробу протидії проапоптотичному середовищу, яке зазвичай спостерігається у вікових скелетних м'язів.
Іншим потенційним засобом для функціонування IL-15 в антиапоптотичній ролі може бути результат його асоціації з антиапоптотичним білком Bcl-2 (30, 41). Відбувається зменшення відсотка CD8 + Т-клітин у мишей IL-15Rα -/-, і це частково зумовлено зменшенням експресії Bcl-2 (41). Екзогенний IL-15 підвищує рівень Bcl-2 у цих клітинах і сприяє зменшенню загибелі клітин при активації (41). Крім того, було показано, що ВІЛ-специфічні CD8 + Т-клітини демонструють знижений рівень Bcl-2. Коли ці клітини культивували з IL-15, експресія Bcl-2 зростала, і це було пов'язано з послабленням апоптозу культур CD8 + Т-клітин (30). Показано, що експресія мРНК та вміст білка в Bcl-2 зростають у старечих скелетних м'язах та у відповідь на атрофічні подразники (32, 35). Хоча ці результати не показують прямої опосередкованої Bcl-2 антиапоптотичної ролі для IL-15, ця можливість вимагає подальшого дослідження.
ГС у гризунів.
Модель розвантаження HS широко застосовувалася у гризунів для вивчення впливу розвантаження на кістки (22) та м’язи (2, 3, 16, 38). У поточному дослідженні та інших (3, 24, 32) HS використовували для вивчення взаємодії старіння та розвантаження. Втрата м’язової маси та сили, пов’язана зі старінням (тобто саркопенія), посилюється при бездіяльності (39). М’язова маса зменшується на ~ 40% у віці від 20 до 60 років, а сила зменшується на 20–40% (розглянуто в посиланні 12). Поточне дослідження узгоджується з попередніми висновками, що показують, що старі скелетні м'язи по-різному реагують на розвантаження порівняно з скелетними м'язами молодих дорослих (24, 32, 35).
Результати цього дослідження відрізняються від попередніх звітів нашої лабораторії, які продемонстрували більшу втрату м'язів у вікових щурів FBN, ніж у молодих дорослих щурів після ГС (3). Варіабельність реакцій тварин на ГС може відбуватися навіть у тій самій лабораторії (16). Наприклад, Fitts et al. (16) повідомили про варіабельність атрофії підошви та пікового ізометричного тетанічного напруження у відповідь на 1 та 2 тижні HS. Автори припустили, що мінливість цих даних може бути спричинена різноманітними реакціями в рухах тварин або порушеннями навколишнього середовища, що призводять до випадкових скорочень м'язів. Метод ГС призводить до розвантаження кінцівок із залишеною недоторканою м’язовою іннервацією, що дозволяє заднім кінцівкам вільно рухатися в просторі. Спочатку активність ЕМГ зменшується, але вона повертається до вихідних рівнів, як тільки через 3 дні після початку ГС (1). У нашому дослідженні тварин перевіряли два рази на день після індукції ГС, спостерігали випадкові скорочення м’язів задньої кінцівки, і це, можливо, сприяло нашим поточним результатам.
На закінчення, мРНК IL-15 конститутивно експресується в скелетних м’язах і реагує як на старіння м’язів, так і на розвантаження кінцівок. Наші дані вказують на те, що старіння є значним стимулом для збільшення експресії мРНК ІЛ-15, оскільки основні наслідки віку спостерігались у всіх обстежених м’язах за допомогою двох моделей старіння та у двох різних видів тварин. Крім того, скелетні м'язи експресують мРНК для функціонального тримерного IL-15R, який би дозволяв трансформувати IL-15 м'язовими клітинами. Можливо, скелетні м'язи реагують на атрофічні подразники збільшенням рівня IL-15, що виділяється як традиційний цитокін, або поданням IL-15 на сарколему, пов'язану з IL-15R. У майбутніх експериментах слід вивчити прямі наслідки модуляції системи IL-15/IL-15R у відповідь на атрофічні подразники як засіб для збереження м’язової маси зі старінням та під час періодів відмови або травми/захворювання м’язів.
Це дослідження було підтримано Національним інститутом гранту на старіння R01 AG-021530 (для С. Е. Олвея) та Американським коледжем спортивної медицини, грантом для докторантів RFG-14 (для Е. Е. Пістіллі).
- Харчування медоносних бджіл - Американський журнал бджіл
- Довготривале обмеження калорій покращує клітинні процеси контролю якості скелетних м’язів людини
- Піші прогулянки з діабетом Журнал Американської медичної асоціації подіатричної медицини Allen Press
- Високопродуктивний скринінг для виявлення інгібіторів ферментів Журнал медичної хімії
- HIIT Найкраща вправа, щоб накачати старі м’язи, чималі