Пневмонектомія VATS та резекції карінальних рукавів - повний торакоскопічний та уніпортальний підхід
Павло Кононець 1, Дмитро Сехняїдзе 2
Внески: (I) Концепція та дизайн: К Павел; (II) Адміністративна підтримка: Московська онкологічна лікарня, Тюменська обласна клінічна лікарня; (III) Надання навчальних матеріалів або пацієнтів: відсутні; (IV) Збір та збір даних: Усі автори; (V) Аналіз та інтерпретація даних: Усі автори; (VI) Написання рукописів: Усі автори; (VII) Остаточне затвердження рукопису: Усі автори.
Ключові слова: Торакоскопічна пневмонектомія; повний торакоскопічний та уніпортальний підхід; рукава каринальної резекції; торакоскопічна лімфаденектомія середостіння
Отримано: 12 грудня 2017 р .; Прийнято: 20 березня 2018 р .; Опубліковано: 17 травня 2018 р.
У перевагах торакоскопічної резекції легень не можна сумніватися, і це підтверджується численними дослідженнями (1-6). Ці процедури дозволяють значно зменшити хірургічну травму та крововтрату, зменшити тривалість перебування в лікарні та зменшити потребу в анестетиках. Інші переваги включають раннє одужання, швидку реабілітацію та поліпшення якості життя. Більше того, при необхідності може бути проведена допоміжна хіміотерапія раніше.
Незважаючи на високий рівень захворюваності на рак легенів у світі та на той факт, що більшість пацієнтів страждає II стадією або, переважно, III стадією захворювання, протягом останніх років спостерігається зменшення кількості пневмонектомій. Це пояснюється новими неоад'ювантними схемами лікування, які нещодавно увійшли в дію, а також акцентом на органозберігаючих операціях з ангіопластикою та бронхопластикою. Однак для деяких пацієнтів з центрально розташованими пухлинами легенів або з інфільтрацією пухлини в суглобових структурах або міждолевою щілиною єдиною можливою хірургічною процедурою є радикальна пневмонектомія. Однією з основних проблем підбору пацієнтів для торакоскопічної пневмонектомії є недоступність пальпації та відсутність повної інтраопераційної ревізії для оцінки поширення пухлини. Як для оцінки поширення пухлини за допомогою пальпації, так і для видалення великих зразків, Деттербек та його колеги запропонували використовувати субстернальний підхід, який дозволяє ввести руку хірурга в грудну клітку (7).
Отримавши більше досвіду в торакоскопічних втручаннях, ряд відеоасистентних пневмонектомій не суттєво збільшився. У 2006 році Деммі та ін. повідомили про 7 торакоскопічних пневмонектомій із 25, виконаних протягом 2 років. Центральні пухлини розміром менше 5 см, інфільтрація центральної частини тріщини, неможливість проведення будь-якої процедури бронхо-ангіопластики та синхронні іпсилатеральні пухлини послужили основними показаннями до радикальної пневмонектомії. Процедура включала проби середостіння або лімфаденектомію. За 4 роки ця ж група авторів опублікувала результати лікування ще для 24 пацієнтів, які перенесли торакоскопічну пневмонектомію з 25% конверсії. Переваги торакоскопічних операцій були пов’язані лише з тривалістю перебування та кількістю крововтрати, яка, як виявилося, була значно нижчою. Що стосується рівня виживання, автори ще не дійшли чітко визначеного висновку, вказуючи на те, що вони не гірші, ніж у відкритих хірургічних операціях. На додаток до операцій на раку легенів, було лише кілька згадувань про використання торакоскопічної пневмонектомії при лікуванні емфіземи легенів і гістоплазмозу легенів (18-21).
У 2014 році Кім та співавтори повідомили про результати семи операцій, проведених протягом 4 років. Середній час роботи становив 6 годин (від 4 до 12 годин). Найдовше потрібно тим пацієнтам, які раніше перенесли операцію через наявність плевральних спайок. Кількість крововтрати варіювала від 150 до 700 мл. У двох пацієнтів розвинувся свищ кукси бронха протягом першого післяопераційного тижня та через 4 місяці. Автори приписують відносно велику кількість ускладнень часу придбання методу та невеликій кількості пацієнтів (22).
Незважаючи на загальну реалізацію торакоскопічних технологій у лікуванні раку легенів (лобектомія та сегментектомія), існує відносно невелика кількість лікарень, що застосовують торакоскопічний підхід для пневмонектомії (23-27). Тим не менше, деякі клініки націлені на зменшення хірургічної травми під час травматичних операцій шляхом пошуку нових малоінвазивних методів, таких як роботизована та однопортова пневмонектомія, включаючи резекцію каріналу (28-31). Хоча однопортовий підхід до пневмонектомії досить складний у виконанні, досвідчені торакальні хірурги виконують ці процедури із задовільними первинними та довгостроковими результатами (32,33).
Маючи на увазі, що онкологічні принципи в торакоскопічній хірургії подібні до принципів відкритої, у цій статті ми зупинимося на важливих технічних подробицях торакоскопічної пневмонектомії, що проводиться за повного торакоскопічного та уніпортального підходу.
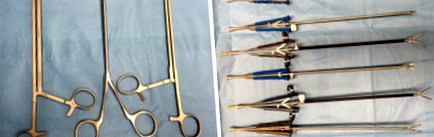
Спеціальний набір торакоскопічних інструментів використовується для торакоскопічних основних резекцій легень, а також відеосистеми Full HD, 4K або 3D, степлерів та машинок (Малюнок 1).
Пацієнта розміщують у бічному пролежні. У проекції V міжреберя ролик піднятий на 5–10 см, а кут операційного столу становить приблизно 150 градусів. У випадку однопортального підходу хірург завжди стоїть перед пацієнтом (Рисунок 2А).
Під час повністю ендоскопічної лівої пневмонектомії хірург також стоїть перед пацієнтом, тоді як під час правої позаду нього (Малюнок 2B). Необхідною умовою є те, що пацієнт знерухомлюється ремінцями безпеки або надувним матрасом для забезпечення безпечних нахилів операційного столу.
Беручи до уваги необхідність вилучення великого зразка, ми змінили положення грудних портів. Для розтину та розподілу голанових структур, а також для отримання візуального зображення операційного поля використовуються три порти, розташовані в центральній частині геміторакса.
При повністю торакоскопічному підході перший порт (оптичний) робиться в V міжребер'ї вздовж передньої пахвової лінії. Після торакоскопічної ревізії плевральної порожнини за схемою розмічаються оптимальні положення решти портів. Потім асистент виконує витягування легенів вгору. Легенева зв’язка і середостінна плевра розкриваються спереду і ззаду від хілуму. Передню медіастінотомію проводять до рівня артеріальної зв’язки вздовж діафрагмального нерва з видаленням лімфатичних вузлів між легеневими венами. Задня стінка верхньої легеневої вени відокремлюється від бронху верхньої частки і береться на судинну стрічку (Малюнок 3А, В).
Після цього ми продовжуємо лімфаденектомію заднього відділу гомілки та підкірка, для якої, здається, варто використовувати ендо-ретрактори, оскільки вони забезпечують хороший доступ до заднього середостіння завдяки тязі лівої легені спереду. Шви ретрактора можна було витягти через отвори троакарів, а також через прокол стінки грудної клітки тонкою голкою. Гак та гармонічний скальпель використовуються для трансекції середостінної плеври, що покриває аорту та задню поверхню хілуму. Середній відділ грудного відділу стравоходу визначається вздовж і відокремлюється від задньої стінки перикарда та від блоку лімфатичних вузлів №7 до протилежного плеврального мішка та перетинчастої частини трахеї. Одночасно ліві бронхіальні артерії, підняті з грудної аорти, підсікаються та перерізаються (Малюнок 4А). Після цього асистент виконує тракцію стравоходу вгору і назад, тим самим даючи простір для розсічення лімфатичних вузлів. Потім ми розтинаємо нижній край лівого головного бронха, задню стінку перикарда, медіальну стінку правого головного бронха та карин. На цьому етапі необхідно запобігти контакту перетинчастої частини трахеї та головних бронхів з активним лезом гармонічного скальпеля. Остаточний вигляд субкаринальної зони показаний на малюнку 4B.
Для забезпечення максимальної тяги лівого головного бронха для здійснення короткого куксу бронха важливо мобілізувати стравохід від перетинчастої частини до рівня дуги аорти. Трахеобронхіальні та субаортальні лімфатичні вузли видаляються одночасно. На цьому етапі холодні ножиці та дисектор є найкращими варіантами дисекції, щоб мінімізувати ризик повторного пошкодження гортанного лівого лівого нерва (Малюнок 5A, B).
У випадку правої пневмонектомії лімфаденектомія середостіння включає гомілкову (# 10), субкаринальну (# 7) та праву паратрахеальні станції лімфатичних вузлів (# 2R і # 4R). Слід зазначити, що при видаленні блоку вузлів важливо зберегти кровопостачання стінки трахеї та головних бронхів для оптимальних умов загоєння кукси бронха або трахеобронхіального анастомозу (Рисунок 6А, Б).
Щоб забезпечити доступ до головного стовбура лівої легеневої артерії, ми розглядаємо питання, починаючи з розтину верхньої легеневої вени. Після цього зберігається розтин та скріплення артерії (Рисунок 7).
Нижня легенева вена розрізається останньою. Лімфаденектомія середостіння, проведена на першому етапі операції, дозволяє отримати вільний доступ до мобілізованого головного бронха. Для того, щоб забезпечити безперебійну техніку на лівому головному бронсі, необхідно повністю мобілізувати роздвоєння головних бронхів та трахеї. Максимальна тяга забезпечується ендоскопічним затискачем або стрічкою. Залежно від підходу, степлер вставляється через X міжребер'я або передній отвір, згинаючись так, щоб вісь його картриджа повинна бути паралельна осі протилежного головного бронха. Щелепи степлера слід розміщувати в передньо-задньому напрямку. Важливим технічним моментом є використання електромеханічного степлера для забезпечення плавного зшивання стінки бронха. Переважно використовувати картридж з максимальною висотою хірургічного затиску та з системою, що забезпечує плавне стиснення на шовній лінії (рис. 8). Остаточний вигляд легеневого відділу та середостіння після торакоскопічної пневмонектомії показано на малюнку 9.
Після завершення анастомозу проводять тест на пухирці води на герметичність. У всіх випадках ми намагаємося покрити анастомоз середостінним або діафрагмальним клаптем. З нашої точки зору, діафрагмовий клапан є більш надійним, але його розтин вимагає більше часу. За допомогою гармонічного скальпеля клапоть утворюється з медіальної частини діафрагми. Потік крові зберігається завдяки діафрагмальним судинам. Клапоть покритий і закріплений окремими швами до лінії трахеобронхіального анастомозу. Дефект діафрагми зашитий за допомогою безперервного V-loc (малюнок 11).
Зразок добувають у захисному контейнері через один порт або через подовжений до 5 см порт у міжребер'ї X. Плевральна порожнина дренується одним дренажем (рисунок 12).
Висновки
Торакоскопічний доступ має багато великих переваг; він відносно збережений, набагато менш травматичний і забезпечує хорошу візуалізацію. Досвід ендоскопічної хірургії дозволяє значно розширити показання до торакоскопічних процедур. У той же час спостерігається тенденція до щадної операції на легенях, зменшення кількості пневмонектомій, що накладає обмеження на проведення малоінвазивних процедур у цієї групи пацієнтів. Сьогодні основним показанням до торакоскопічної процедури є рак легень І – ІІ стадій, коли можливо провести сегментектомію або лобектомію. Тим не менше, існує невелика група пацієнтів, для яких бронхо-ангіопластика неможлива і які потребують радикального видалення легенів часто з резекцією оточуючих структур та резекціями кардинальних рукавів. Беручи до уваги проблеми з інтраопераційною ревізією, пацієнтів слід ретельно відібрати для пневмонектомії. У той же час невелика кількість повідомлень про торакоскопічну пневмонектомію в літературі показує допустимий рівень ускладнень. Враховуючи однакову лімфаденектомію у відкритій та ендоскопічній хірургії, слід очікувати подібних віддалених результатів, які слід проаналізувати в майбутньому.
Подяка
Виноска
Конфлікт інтересів: Автори не мають заявляти про конфлікт інтересів.
- Дослідження ефективності тренувань на джгутах - Повний текст
- РОЛЬ МНОГОФАКТОРІАЛЬНОГО ПІДХОДУ ДО ЛІКУВАННЯ ОЖИРІННЯ В ІП Ingenta Connect
- Складання транскриптомів із давно прочитаних вирівнювань РНК-послідовностей із повним текстом біології геному StringTie2
- Тайський суп з детоксикації шпинату Легкий рецепт лужний; Повна поживних речовин
- Жінка втрачає половину ваги тіла після перенесеної операції на шлунковому рукаві в Мексиці