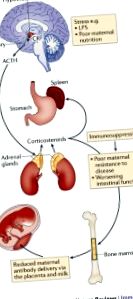
Як харчування та материнська мікробіота формують імунну систему новонароджених
Предмети
Ключові моменти
Сама материнська мікробіота впливає на розвиток плода та новонародженого.
Метаболічний вплив плода внутрішньоутробно залежить від харчування матері та впливу ксенобіотиків, які обидва модулюються мікробним метаболізмом.
Молекули, що походять від кишкових мікроорганізмів матері, потрапляють до її нащадків через плаценту під час внутрішньоутробного розвитку та через материнське молоко у постнатальний період.
Материнські антитіла посилюють мікробний молекулярний перенос і того, і іншого внутрішньоутробно і під час лактації.
Повідомлення від материнських мікробних молекул формує розвиток та функцію імунної системи в ранньому віці.
Анотація
Поверхні слизової оболонки ссавців щільно колонізовані мікроорганізмами, які зазвичай називають коменсальною мікробіотою. Вважається, що плід внутрішньоутробно є стерильним, і колонізація мікроорганізмами починається лише після народження. Тим не менше, ненароджений плід піддається дії безлічі метаболітів, що походять від коменсальної мікробіоти матері, які досягають системних ділянок материнського тіла. Мікробіота кишечника сильно персоналізована і під впливом факторів навколишнього середовища, включаючи харчування. Члени материнської мікробіоти можуть метаболізувати дієтичні компоненти, фармацевтичні препарати та токсини, які згодом можуть передаватися розвиваючомуся плоду або новонародженому, що годує груддю. У цьому огляді ми обговорюємо складну взаємодію між харчуванням, материнською мікробіотою та проковтнутими хімічними речовинами та узагальнюємо їх вплив на імунітет у нащадків.
Параметри доступу
Підпишіться на журнал
Отримайте повний доступ до журналу протягом 1 року
лише 4,60 € за випуск
Усі ціни вказані у нетто-цінах.
ПДВ буде додано пізніше під час оплати.
Оренда або купівля статті
Отримайте обмежений за часом або повний доступ до статей на ReadCube.
Усі ціни вказані у нетто-цінах.
Список літератури
Блекберн, Д. Г. Реконструкція еволюції живучості та плацентації. Дж. Теор. Біол. 192, 183–190 (1998).
Ренфрі, М. Б., Хоре, Т. А., Шоу, Г., Грейвс, Дж. А. і Паск, А. Дж. Еволюція геномного імпринтингу: уявлення про сумчастих і монотремах. Анну. Преподобний Genomics Hum. Genet. 10, 241–262 (2009).
Millen, J. W. & Woollam, D. H. Материнське харчування стосовно аномального розвитку плода. Proc. Nutr. Соц. 19, 1–5 (1960).
Пача, Дж. Розвиток транспортної функції кишечника у ссавців. Фізіол. Преподобний. 80, 1633–1667 (2000).
Тороу, Н. та Горнеф, М. В. Неонатальне вікно можливостей: підготовка до життєвої взаємодії господар-мікроб та взаємодії імунного гомеостазу. J. Імунол. 198, 557–563 (2017). Ця стаття елегантно узагальнює літературу про важливість періоду часу незабаром після народження для формування імунної системи людини, її корінної коменсальної мікробіоти та сприйнятливості до хвороби в подальшому житті.
Букліяс, Т. Харчування, ріст і час: дослідження Елсі Віддовсон і Роберта Макканса щодо пренатального та раннього постнатального росту. Студ. Hist. Філос. Біол. Біомед. Наук. 47, 267–277 (2014).
Уолтон, А. та Хаммонд, Дж. Вплив матері на ріст та конформацію у схрещуваннях коней Шир-Шетландські Поні. Proc. Р. Соц. B 125, 311–335 (1938).
Росс, М. Г. та Білл, М. Х. Дорослі наслідки обмеження внутрішньоутробного росту. Семін. Перинатол. 32, 213–218 (2008).
Фолл, К. Х. Докази внутрішньоматкового програмування ожиріння в подальшому житті. Енн Гул. Біол. 38, 410–428 (2011).
Равеллі, А. С. та співавт. Толерантність до глюкози у дорослих після пренатального впливу голоду. Ланцет 351, 173–177 (1998).
Деннісон, Е. М. та співавт. Вага при народженні, генотип рецептора вітаміну D та програмування остеопорозу. Педіатр. Перинат. Епідеміол. 15, 211–219 (2001).
Томпсон, C., Syddall, H., Rodin, I., Osmond, C. & Barker, D. J. Вага при народженні та ризик депресивного розладу в пізньому віці. Br. J. Психіатрія 179, 450–455 (2001).
Бейтсон, П. та співавт. Пластичність розвитку та здоров’я людини. Природа 430, 419–421 (2004).
Ho, S. M., Tang, W. Y., Belmonte de Frausto, J. & Prins, G. S. Розвиток впливу естрадіолу та бісфенолу А підвищує сприйнятливість до канцерогенезу простати та епігенетично регулює фосфодіестеразу типу 4, варіант 4. Рак Res. 66, 5624–5632 (2006).
Zinkernagel, R. M. Материнські антитіла, дитячі інфекції та аутоімунні захворювання. Н. Енгл. J. Med. 345, 1331–1335 (2001).
Kearney, J. F., Patel, P., Stefanov, E. K. & King, R. G. Репертуари природних антитіл: розвиток та функціональна роль у гальмуванні алергічних захворювань дихальних шляхів. Анну. Преподобний Імунол. 33, 475–504 (2015).
Newbold, R. R. Уроки, отримані внаслідок перинатального впливу діетилстильбестролу. Токсикол. Заяв. Фармакол. 199, 142–150 (2004).
Бретон, Дж. Та ін. Мікробіота кишечника обмежує навантаження важких металів, спричинене хронічним впливом всередину. Токсикол. Lett. 222, 132–138 (2013).
Вільсон, І. Д. та Ніколсон, Дж. К. Взаємодія мікробіомів кишечника з метаболізмом лікарських засобів, ефективністю та токсичністю. Transl Res. 179, 204–222 (2017).
Палмер, А. С. Програмування імунної системи, що розвивається, за допомогою харчування. Адв. Nutr. 2, 377–395 (2011).
Chen, X., Welner, R. S. & Kincade, P. W. Можливий внесок ретиноїдів у регуляцію В-лімфопоезу плода. Євро. J. Імунол. 39, 2515–2524 (2009).
ван де Паверт, С. А. та ін. Материнські ретиноїди контролюють вроджені лімфоїдні клітини 3 типу та встановлюють імунітет потомства. Природа 508, 123–127 (2014).
Fraker, P. J. & King, L. E. Перепрограмування імунної системи під час дефіциту цинку. Анну. Преподобний Нутр. 24, 277–298 (2004).
Benediktsson, R., Calder, A. A., Edwards, C. R. & Seckl, J. R. Плацентарна 11β-гідроксистероїддегідрогеназа: ключовий регулятор експозиції глюкокортикоїдів плоду. Клін. Ендокринол. (Oxf.) 46, 161–166 (1997).
Backhed, F. et al. Мікробіота кишечника як фактор навколишнього середовища, що регулює накопичення жиру. Proc. Natl Акад. Наук. США 101, 15718–15723 (2004). Це важливий документ, який повідомляє про всеохоплюючі метаболічні наслідки мікробного обміну та молекулярного обміну для господаря.
Холмс, Е., Лі, Дж. В., Атанасіу, Т., Ашрафіян, Х. та Ніколсон, Дж. К. Розуміння ролі порушення мікробіому кишечника – метаболічного сигналу господаря у здоров’ї та захворюваннях. Тенденції мікробіол. 19, 349–359 (2011).
Mandal, S. та співавт. Прийом жиру та вітамінів під час вагітності має сильніші стосунки з прозапальною мікробіотою матері, ніж споживання вуглеводів. Мікробіом 4, 55 (2016).
Кларк, А. та Мах, Н. Роль вітаміну D у гігієнічній гіпотезі: взаємодія між вітаміном D, рецепторами вітаміну D, мікробіотою кишечника та імунною відповіддю. Спереду. Імунол. 7, 627 (2016).
Holmes, E., Li, J. V., Marchesi, J. R. & Nicholson, J. K. Склад і активність мікробіоти кишечника стосовно метаболічного фенотипу хазяїна та ризику захворювання. Cell Metab. 16, 559–564 (2012).
Ma, J. та співавт. Дієта матері з високим вмістом жиру під час вагітності постійно змінює мікробіом нащадків у моделі приматів. Нат. Комун. 5, 3889 (2014).
Рідігер, В. Е. Роль анаеробних бактерій у метаболічному добробуті слизової оболонки товстої кишки у людини. Кишечник 21, 793–798 (1980).
Фурусава, Ю. та ін. Бутират, отриманий коменсальним мікробом, індукує диференціювання регуляторних Т-клітин товстої кишки. Природа 504, 446–450 (2013).
Арпая, Н. та ін. Метаболіти, вироблені коменсальними бактеріями, сприяють генерації периферичних регуляторних Т-клітин. Природа 504, 451–455 (2013). Посилання 31–33 показують чіткий вплив мікробних метаболітів на імунний розвиток та функцію господаря.
Сміт, П. М. та ін. Мікробні метаболіти, коротколанцюгові жирні кислоти, регулюють гомеостаз клітин Treg у товстій кишці. Наука 341, 569–573 (2013).
ЛеБлан, Дж. Г. та ін. Бактерії як постачальник вітаміну своєму господареві: перспектива мікробіоти кишечника. Curr. Думка. Біотехнол. 24, 160–168 (2013).
Шульман, С. Г. Основи взаємодії іонізуючих випромінювань з хімічними, біохімічними та фармацевтичними системами. Дж. Фарм. Наук. 62, 1745–1757 (1973).
Альберт, М. Дж., Матан, В. І. та Бейкер, С. Дж. Синтез вітаміну В12 бактеріями тонкої кишки людини. Природа 283, 781–782 (1980).
Каміло, Е. та ін. Фолат, синтезований бактеріями у верхній частині тонкої кишки людини, засвоюється господарем. Гастроентерологія 110, 991–998 (1996).
Collado, M. C., Isolauri, E., Laitinen, K. & Salminen, S. Виразний склад мікробіоти кишечника під час вагітності у жінок із надмірною вагою та нормальною вагою. Am. J. Clin. Nutr. 88, 894–899 (2008).
Корен, О. та ін. Реконструкція мікробіома кишечника та метаболічні зміни під час вагітності. Клітинка 150, 470–480 (2012).
Россант, Дж. І Крос, Дж. С. Розвиток плаценти: уроки від мутантів мишей. Нат. Преподобний Genet. 2, 538–548 (2001).
Сулік, К. К. Генез індукованого алкоголем краніофаціального дисморфізму. Досвід. Біол. Мед. (Мейвуд) 230, 366–375 (2005).
Гільберт, Дж. М., Нінг, Дж., Симчовіч, С. та Зампаліоне, Н. Плацентарний перенос квазепаму у мишей. Drug Metab. Диспозиції. 14, 310–312 (1986).
Коан, П. М. та ін. Адаптація плацентарної здатності переносити поживні речовини для задоволення потреб росту плода залежить від розміру плаценти у мишей. J. Physiol. 586, 4567–4576 (2008).
Констанція, М. та співавт. Плацентарний IGF-II є основним модулятором росту плаценти та плоду. Природа 417, 945–948 (2002).
Лі, Л. та співавт. Регулювання поведінки матері та зростання нащадків за батьківською мовою Кілочок3. Наука 284, 330–333 (1999).
Heijmans, B. T. та співавт. Стійкі епігенетичні відмінності, пов'язані з пренатальним впливом голоду у людей. Proc. Natl Акад. Наук. США 105, 17046–17049 (2008).
Еггерт, Х., Курц, Дж. & Дідденс-де-Бур, М.Ф. Proc. Біол. Наук. 281, 20142089 (2014).
Кох, М. А. та ін. Материнські антитіла IgG та IgA пригнічують реакцію Т-хелперів слизової оболонки у ранньому віці. Клітинка 165, 827–841 (2016). Це дослідження демонструє присутність материнських мікробіотичних специфічних IgG та IgA в материнському молоці та показує, що вони передаються потомству для встановлення функціонального мутуалізму з надходить мікробіоти.
Grindstaff, J. L., Brodie, E. D. 3rd & Ketterson, E. D. Імунна функція між поколіннями: механізм інтеграції та еволюційний процес при передачі материнських антитіл. Proc. Біол. Наук. 270, 2309–2319 (2003).
Gautreaux, M. D., Deitch, E. A. & Berg, R. D. Т-лімфоцити в захисті господаря від транслокації бактерій із шлунково-кишкового тракту. Заразити. Імунний. 62, 2874–2884 (1994).
O'Boyle, C. J. et al. Мікробіологія транслокації бактерій у людини. Кишечник 42, 29–35 (1998).
Perez, P. F. та співавт. Бактеріальне відбиття імунної системи новонароджених: уроки з материнських клітин? Педіатрія 119, e724 – e732 (2007).
Fardini, Y., Chung, P., Dumm, R., Joshi, N. & Han, Y. W. Передача різноманітних ротових бактерій до мишачої плаценти: докази мікрофлори в роті як потенційного джерела внутрішньоутробної інфекції. Заразити. Імунний. 78, 1789–1796 (2010).
Яджима, М. та ін. Транслокація бактерій у новонароджених щурів: зв’язок між кишковою флорою, транслокованими бактеріями та впливом молока. J. Педіатр. Гастроентерол. Nutr. 33, 592–601 (2001).
Аагаард, К. та ін. У плаценті є унікальний мікробіом. Наук. Transl Med. 6, 237ra65 (2014). Це дослідження демонструє наявність непатогенних коменсальних бактерій у зразках плаценти людини.
Goldenberg, R. L., Hauth, J. C. & Andrews, W. W. Внутрішньоутробна інфекція та передчасні пологи. Н. Енгл. J. Med. 342, 1500–1507 (2000).
Сміт, К., Маккой, К. Д. та Макферсон, А. Дж. Використання аксенових тварин при вивченні адаптації ссавців до їх коменсальної кишкової мікробіоти. Семін. Імунол. 19, 59–69 (2007).
Hapfelmeier, S. та співавт. Оборотна мікробна колонізація безмікробних мишей виявляє динаміку імунних відповідей IgA. Наука 328, 1705–1709 (2010).
Гомес де Агуеро, М. та ін. Материнська мікробіота рухає ранній постнатальний вроджений імунний розвиток. Наука 351, 1296–1302 (2016). Ця стаття описує механізм, за допомогою якого гестаційна колонізація матері формує склад та функції імунної системи раннього віку.
Jacobowitz Israel, E., Patel, V. K., Taylor, S. F., Marshak-Rothstein, A. & Simister, N. E. J. Імунол. 154, 6246–6251 (1995).
Малек, А., Сагер, Р., Кун, П., Ніколаїдес, К. Х. та Шнайдер, Х. Еволюція матнофетального транспорту імуноглобулінів під час вагітності людини. Am. Дж. Репрод. Імунол. 36, 248–255 (1996).
Neu, J. Розвиток шлунково-кишкового тракту та задоволення харчових потреб недоношених дітей. Am. J. Clin. Nutr. 85, 629S – 634S (2007).
Siggers, R. H., Siggers, J., Thymann, T., Boye, M. & Sangild, P. T. Харчова модуляція мікробіоти та кишкової мікрофлори кишечника у недоношених новонароджених, сприйнятливих до некротизуючого ентероколіту. Дж. Нутр. Біохім. 22, 511–521 (2011).
Kramer, D. R. & Cebra, J. J. Рання поява «природних» слизових IgA-відповідей та зародкових центрів у мишей-сисунів, що розвиваються за відсутності материнських антитіл. J. Імунол. 154, 2051–2062 (1995).
Харріс, Н. Л. та співавт. Механізми захисту антитіл слизових новонароджених. J. Імунол. 177, 6256–6262 (2006).
Rogier, E. W. та співавт. Секреторні антитіла в грудному молоці сприяють довгостроковому гомеостазу кишечника шляхом регулювання мікробіоти кишечника та експресії гена хазяїна. Proc. Natl Акад. Наук. США 111, 3074–3079 (2014). Це дослідження дає чіткі докази того, що материнські антитіла в грудному молоці виконують захисну роль у нащадків.
Кау, А. Л. та ін. Функціональна характеристика бактеріальних таксонів, орієнтованих на IgA, від недоїдаючих малавійських дітей, які виробляють ентеропатію, залежну від дієти. Наук. Transl Med. 7, 276ra24 (2015). Це ключовий документ, що демонструє взаємодію між мікробіотиками людської дитини та їх імунною системою, що визначають кишкову ентеропатію, яка є серйозною та загалом недооціненою проблемою у країнах, що розвиваються, що впливає на довгостроковий розвиток та здоров'я постраждалих людей.
Блантон, Л. В. та ін. Бактерії кишечника, які запобігають порушення росту, що передаються мікробіотою від недоїдаючих дітей. Наука 351, aad3311 (2016).
Waterland, R. A. & Jirtle, R. L. Транспонсовані елементи: мішені для раннього поживного впливу на епігенетичну генну регуляцію. Мол. Клітинка. Біол. 23, 5293–5300 (2003).
Burris, H. H. та співавт. Метилювання ДНК потомства гена-репресора арил-вуглеводневих рецепторів пов'язане з ІМТ матері, терміном вагітності та вагою при народженні. Епігенетика 10, 913–921 (2015).
McGill, J. та співавт. Вплив етанолу на плід має тривалий вплив на тяжкість інфекцій вірусу грипу. J. Імунол. 182, 7803–7808 (2009).
Lee, G. R., Kim, S. T., Spilianakis, C. G., Fields, P. E. & Flavell, R. A. T хелперна диференціація клітин: регуляція цис елементи та епігенетика. Імунітет 24, 369–379 (2006).
Schuyler, R. P. та співавт. Виразні тенденції моделювання метилювання ДНК у вродженій та адаптивній імунній системі. Клітинний представник. 17, 2101–2111 (2016).
Липка, Д. Б. та ін. Ідентифікація змін метилювання ДНК при цис-регуляторні елементи на ранніх етапах диференціації HSC за допомогою послідовності цільного геному бісульфіту на основі тегування. Клітинний цикл 13, 3476–3487 (2014).
Cabezas-Wallscheid, N. et al. Ідентифікація регуляторних мереж у HSC та їх безпосереднє потомство за допомогою інтегрованого аналізу протеомів, транскриптомів та ДНК метилому. Клітинна стовбурова клітина 15, 507–522 (2014).
Кротики, Л. та співавт. Бактеріальне різноманіття в меконії недоношених новонароджених та еволюція їх калової мікробіоти протягом першого місяця життя. PLOS ONE 8, e66986 (2013).
Arrieta, M. C., Stiemsma, L. T., Amenyogbe, N., Brown, E. M. & Finlay, B. Мікробіом кишечника в ранньому віці: здоров’я та хвороби. Спереду. Імунол. 5, 427 (2014).
Backhed, F. et al. Динаміка та стабілізація мікробіому кишечника людини протягом першого року життя. Клітинний мікроб 17, 690–703 (2015).
Подяки
Автори дякують колегам у своїй лабораторії та У. Зауеру, В. Хардту та К. Мюллеру за корисні дискусії на цю тему. Робота А.Дж.М. фінансується за рахунок грантів Швейцарського національного наукового фонду (SNSF 310030B_160262 та SNSF Sinergia CRSII3_154414) та програми Swiss SystemsX (GutX)); М.Г.А. має грант Ambizione Швейцарського національного наукового фонду (PZ00P3_168012); та S.C.G.-V. підтримується довгостроковою стипендією Європейської організації молекулярної біології (ALTF 841–2013).
Інформація про автора
Приналежності
Моріс Мюллер Лабораторії, Департамент Klinische Forschung, Universitätsklinik für Viszerale Chirurgie und Medizin Inselspital, Бернський університет, Муртенштрассе 35, Берн, 3008, Швейцарія
Ендрю Дж. Макферсон, Мерседес Гомес де Агуеро та Стефані К. Ганал-Вонарбург
Ви також можете шукати цього автора в PubMed Google Scholar
Ви також можете шукати цього автора в PubMed Google Scholar
Ви також можете шукати цього автора в PubMed Google Scholar
- Herbalife Nutrition Institute проводить симпозіум з питань харчування та імунної функції на конференції ASN
- Форма харчування насіння конопель
- Посилюючий імунний сидр - Природа; s Виховання
- Закладаючи міцну основу для вашої стратегії Ironman Nutrition
- Вступ до харчування