Хімометричний аналіз 1-ЯМР-спектрів низького поля для розкриття фальсифікації харчових добавок для схуднення фармацевтичними сполуками
Пов’язані дані
Анотація
1. Вступ
На сьогодні фальсифікація дієтичних добавок (ДБ) схваленими чи не затвердженими ліками представляє загрозу здоров’ю споживачів [1]. Проблема фальсифікації препаратів для схуднення активними фармацевтичними інгредієнтами для посилення їх дії є широко поширеною проблемою [2]. Два найпоширеніші долюгенти, виявлені в препаратах для схуднення, - це сибутрамін та фенолфталеїн, окремо або в комбінації [3,4,5]. Сибутрамін - це аноректичний препарат, який був вилучений з ринку багатьох країн (Європейський Союз, США, Китай, Австралія, Індія…) з 2010 року через проблеми із серцево-судинною системою. Фенолфталеїн застосовується завдяки його проносним властивостям, навіть незважаючи на те, що він був вилучений з безрецептурних продуктів наприкінці 1990-х років через канцерогенний ризик [6].
Для виявлення та/або кількісної оцінки недекларованих лікарських засобів при схудненні ДС запропоновані різні аналітичні методи. Найбільш часто описувана техніка - це рідинна хроматографія з ультрафіолетовим, діодним масивом або мас-спектрометрією [7,8,9]. Запропоновано інші методи, включаючи вібраційну спектроскопію [10], газову хроматографію [4] або іонообмінну хроматографію з виявленням провідності [11]. 1-ЯМР-спектроскопія високого поля (ВЧ) також була успішно застосована для виявлення та кількісної оцінки адлювантів при DS для схуднення [5].
ЯМР із низьким полем (НЧ) - нова технологія, заснована на використанні компактного ЯМР нового покоління [12,13,14]. Нещодавно було описано кілька застосувань ЯМР НЧ у фармацевтичній галузі [15,16,17,18,19], і продемонстровано можливість ЯМР НЧ для виявлення фальсифікації ДС [15,19].
Метою цього дослідження є поглиблення оцінки ЯМР НЧ для виявлення фальсифікації ДС для схуднення шляхом поєднання даних ЯМР НЧ 1 Н з хіміометричним аналізом, що дозволяє класифікувати зразки без експертної інтерпретації спектрів ЯМР, записаних на недорогій версії. спектрометр. Таким чином, ми проаналізували фальсифіковані та нефальсифіковані DS для схуднення, які якісно та кількісно раніше характеризували HF 1 H ЯМР [5], з LF 1 H ЯМР для створення статистичних моделей, в які вводять дані LF 1 H ЯМР нових зразків. . Обговорюються інтерес та обмеження цього підходу.
2. Результати та обговорення
2.1. LF 1 H ЯМР-аналіз
DS для схуднення, використаний у цьому дослідженні, за винятком нещодавно придбаних тестових зразків (T), раніше були проаналізовані та повністю охарактеризовані HF 1 H ЯМР, тобто природа та кількість домішок в одиницях (капсула, таблетка або саше) були відомі [5]. Повний перелік DS наведено в таблиці S1.
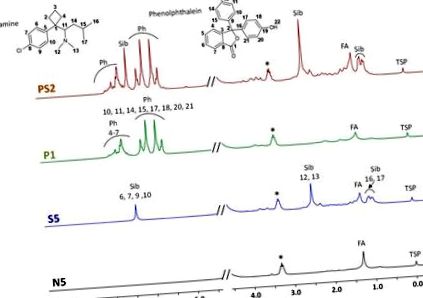
На першому етапі цього дослідження всі DS аналізували в двох примірниках за допомогою LF 1 H ЯМР у дейтерованому метанолі. Час запису кожного спектру становив 15,5 хв, а профілі типових зразків проілюстровані на рисунку 1 .
Типові LF 1 H ЯМР-спектри дієтичних добавок для схуднення, записані при 60 МГц (N, група, що не є фальсифікованою (природною); S, група, фальсифікована сибутраміном; P, група, фальсифікована фенолфталеїном; PS, як фальсифікована група сибутраміну, так і фенолфталеїну ). Ph: Фенолфталеїн; Сіб: сибутрамін; FA: жирні кислоти; TSP: внутрішня довідка; *: CD2HOD.
Хоча спектри ЯМР LF 1 H досить погано розкриті, основні характерні сигнали сибутраміну та фенолфталеїну, двох найпоширеніших пригнічувачів ДС для схуднення, легко виявити окремо або в поєднанні. Як видно на малюнку 1, сибутрамін ідентифікується у зразках S5 та PS2 за сигналами його ароматичних протонів при 7,41 ppm та його метильних груп при 2,49 (CH3 12 та 13) та 1,02 (CH3 16 та 17) ppm. Аналогічним чином, ароматичні протони фенолфталеїну дають характерний малюнок (6,5-8,0 ppm), який можна спостерігати в DS P1 та PS2. Зразок N5 являє собою DS без ад'юланту, і, крім еталонного сигналу та сигналу розчинника, при 1,27 ppm легко виявляється лише сигнал деяких протонів CH2 жирних кислот з рослинних екстрактів. Незначні сигнали, що відповідають ароматичним протонам природних поліфенолів або інших природних сполук, також виявляються в декількох зразках.
2.2. Хімометричний аналіз
Для початку хемометричного аналізу була побудована статистична модель, виконана двокласове порівняння: DS без домішки (природний: N, n = 19) порівнювали з DS, що містив або сибутрамін (S, n = 12), або фенолфталеїн (P n = 9), зразки (S) та (P) розглядаються разом (n = 21) як “фальсифіковані зразки”. Після обробки спектрів (6–8 частин на мільйон, див. Експериментальну частину), групування та нормалізації даних, частковий найменший квадрат-дискримінантний аналіз (PLS-DA) призвів до прогнозної моделі з двома основними компонентами PLS та хорошими критеріями перевірки (Q 2 = 0,61, R 2 Y = 0,76, CV-ANOVA = 2,3 × 10 −18). Усі значення Q 2 та R 2 були нижчими в тесті перестановки, ніж у моделі, що підтверджує її добрі результати. Класифікація всіх зразків була отримана з двокласової моделі на основі прогнозованих значень Y (YpredPS, що є значенням Y, передбаченим моделлю на основі змінних блоку X (інтенсивності резонансу при заданих ppm)), що вказує на ймовірність що зразок належить до одного класу моделі (фальсифікований чи фальсифікований).
Таблиця 1
Класифікаційний список із прогнозованими значеннями Y (YPredPS) для тестових зразків (T) на основі двокласової моделі PLS-DA, побудованої з даними ЯМР LF 1 H та доповненої візуальним спостереженням за проекцією зразків на три класи Модель PLS-DA, показана на малюнку 3 А.
| Т1 | 0,18 | природний | N | - |
| Т2 | 0,37 | прикордонна | P | фенолфталеїн |
| Т3 | 0,16 | природний | N | - |
| Т4 | 0,17 | природний | N | - |
| Т5 | 0,18 | природний | N | - |
| Т6 | 0,79 | фальсифікований | P | фенолфталеїн |
| Т7 | 0,30 | прикордонна | P | фенолфталеїн |
| Т8 | 0,17 | природний | N | - |
| Т9 | 0,45 | фальсифікований | S | сибутрамін |
| Т10 | 0,17 | природний | N | - |
| Т11 | 0,17 | природний | N | - |
| Т12 | 0,69 | фальсифікований | S | сибутрамін |
| Т13 | 0,65 | фальсифікований | S | сибутрамін |
Щоб піти далі в класифікації DS, був проведений новий аналіз PLS-DA, в якому зразки (N), (P) та (S) розглядались як три окремі групи. Отримана хороша модель прогнозування з двома основними компонентами PLS (Q 2 = 0,66, R 2 Y = 0,74), р-значенням CV-ANOVA 3,4 × 10 −21 та успішно проведеним тестом перестановки. Графік балів цього трикласного PLS-DA демонструє чітку дискримінацію між трьома категоріями DS (Рисунок 3 A). Зразки (P) (темно-синій) та (S) (зелений) виглядають більш розповсюдженими, ніж зразки (N) (жовтий), оскільки в кожній пробі міняється кількість змішаної речовини в межах від 8 до 16 мг на одиницю для сибутраміну у зразках S) і від 5 до 55 мг на одиницю для фенолфталеїну у зразках (P) [5].
(A) Діаграма результатів трикласної моделі PLS-DA, побудована на основі ЯМР-спектрів LF 1 H, зразків N (не фальсифікованих), S (фальсифікованих сибутраміном) та P (фальсифікованих фенолфталеїном). Оцінка ділянок (B), (C.) та (D) показують проекцію зразків PS (фальсифікованих як сибутраміном, так і фенолфталеїном), T (тестові зразки) та X (атипові зразки, див. текст) відповідно на побудовану модель (A).
(PS) зразки (фіолетові), спроектовані в цій трикласній моделі PLS-DA, розташовані ближче до (P), ніж до (S) зразків (Малюнок 3 B). Це спостереження узгоджується із більшою кількістю фенолфталеїну порівняно із сибутраміном, що міститься у більшості зразків [5]. Діаграма оцінки проекції тестових зразків (Т) у моделі підтверджує класифікацію, запропоновану в Таблиці 1, але дає більш точний аналіз (Рисунок 3 С). Дійсно, зразки T1, T3–5, T8, T10 і T11 перекриваються з (N) зразками, і тому їх можна вважати природними. Зразки Т9, Т12 і Т13 містять домішку сибутраміну, тоді як зразки Т2, Т6 і Т7 містять фенолфталеїн. Можна помітити, що жоден із зразків (Т) не належить до класу (PS), тобто не містить суміші фенолфталеїну та сибутраміну. Оскільки статистичний аналіз (T) зразків проводився наосліп, тобто без ретельного вивчення їх спектрів ЯМР LF (і HF) 1 H, ці дані були підтверджені візуальним аналізом цих спектрів.
Той факт, що два зразки T2 і T7 розглядались як граничні в класифікації, встановленій із передбачених значень Y попередньої двокласової моделі (табл. 1), але тепер краще характеризуються моделлю трьох класів (рис. 3 С). також можна пояснити візуальним спостереженням їх ЯМР-спектрів LF 1 H. Дійсно, як повідомляється на малюнку 4, сигнали фенолфталеїну виявляються у зразках Т2 та Т7, але з меншим співвідношенням сигнал/шум, ніж у спектрі Р1, через низьку кількість адлюранту в цих ДС. Вище ми згадали, що сигнали, що відповідають ароматичним протонам природних поліфенолів або інших природних сполук, були виявлені в кількох (N) зразках (для ілюстрації, спектр ЯМР LF 1 H зразка N6 показаний на малюнку 4). Їх хімічні зрушення та інтенсивності, близькі до тих, що спостерігаються для фенолфталеїну у зразках Т2 та Т7, призвели до класифікації цих ДС як прикордонних при першому підході (Таблиця 1).
LF 1 H ЯМР-спектри деяких дієтичних добавок для схуднення, записані при 60 МГц. Ph: фенолфталеїн; Сіб: сибутрамін.
На закінчення слід сказати, що трикласний PLS-DA працює добре, оскільки дає змогу правильно прогнозувати природу домішкуватого сибутраміну або фенолфталеїну - двох заборонених препаратів, які найчастіше додають до ДС для схуднення для підвищення їх ефективності. Найнижча межа концентрації фенолфталеїну, виявлена моделлю, становить 3 мг на 100 мг порошку, що відповідає ≈ 6 мг на одиницю, якщо враховувати середню масу вмісту капсули 200 мг. Найнижчої межі концентрації сибутраміну не вдалося досягти, оскільки всі проаналізовані DS мали значення YPredPS> 0,7, дуже далекі від значення 0,3, яке характеризує межу між фальсифікованою та неподробленою DS (рис. 2). Попри помилку класифікації, тим не менш, можливо, якщо домішка або природна сполука має структуру, яка веде до 1 H ЯМР-сигналів у зонах резонансної частоти, які розглядаються для побудови моделі. Наприклад, характерний сигнал метильних протонів 16 і 17 сибутраміну при 1,02 ppm не міг бути використаний для створення моделі, оскільки вона часто перекривалась резонансом жирних кислот.
Це дослідження показує, що застосування хімічної обробки до даних ЯМР LF 1 H є засобом розширення області застосування техніки, зокрема для аналізу складних сумішей. Цей підхід був успішно запропонований у сільськогосподарських продуктах для аналізу та аутентифікації харчових олій [21,22] та м'яса [23]. Зовсім недавно подібний підхід був використаний для аналізу неякісних та фальсифікованих лікарських засобів [19]. Наше дослідження розширює поле до фальсифікації DS, проблеми на перехресті між сільськогосподарською та харчовою продукцією. У випадку фальсифікації DS для схуднення запропонований аналітичний процес може бути корисним для виявлення першої лінії зразків, які можуть бути фальсифікованими, не вдаючись до експертного аналізу спектрів ЯМР 1 H. Підготовка зразків проста і швидка, а отримання ЯМР LF 1 H - це просто, досить кнопково і не вимагає специфічних знань ЯМР. Перспективою цього дослідження було б автоматизувати весь процес, щоб запропонувати метод "під ключ", який можна було б застосувати в лабораторіях контролю якості.
3. Матеріали та методи
3.1. Зразки
Різні групи DS для схуднення замовляли в Інтернеті та аналізували за допомогою LF 1 H ЯМР: (N) без фальсифікації, (S) фальсифікація сибутраміном, (P) фальсифікація фенолфталеїном, (PS) фальсифікація як фенолфталеїном, так і сибутраміном, (T) тестові зразки та (X) два нетипові зразки (таблиця S1). 40 DS, що використовуються для побудови статистичних моделей ((N) (n = 19), (S) (n = 12) та (P) (n = 9)), а також (PS) вибірки (n = 11), а два DS (X) раніше були якісно та кількісно охарактеризовані в нашій лабораторії з HF 1 H ЯМР [5]. Для тестування статистичних моделей у листопаді 2019 року в Інтернеті було придбано 13 нових DS (T1 – T13), які були проаналізовані LF та HF 1 H ЯМР при отриманні.
3.2. Підготовка зразка для LF 1 H ЯМР-аналізу
Близько 100 мг порошкоподібних зразків змішували з 1 мл дейтерованого метанолу під вихровим перемішуванням протягом 15 с, а потім обробляли ультразвуком протягом 5 хв. Потім суспензію центрифугували (5 хв, 3000 об/хв) і супернатант (700 мкл) аналізували. Тридцять мікролітрів 2,2,3,3-тетрадеутеро-3- (триметилсилил) пропаноату натрію (TSP, 40 мМ) як внутрішній еталон хімічного зсуву додавали перед аналізом ЯМР. Кожна DS була підготовлена у двох примірниках.
3.3. LF 1 H ЯМР-аналіз
Якісні спектри ЯМР LF 1 H були отримані на настільному ЯМР-спектрометрі Pulsar ™ (Oxford Instruments, Абінгдон, Великобританія), що працює на частоті 59,7 МГц для 1 H. Температура всередині спектрометра становила 310 К. Програмне забезпечення SpinFlow 1.2.0.1 (Oxford Instruments), обробка виконана за допомогою програми MNova 11.0 (Mestrelab Research, Сантьяго де Компостела, Іспанія). Реєстрації вільних індукційних розпадів (FID) реєстрували з кутом перекидання 90 ° (12,5 мкс), спектральною шириною 5000 Гц (83,75 ppm) та 8 K комплексними точками (час збору 1,64 с). Затримку релаксації встановили на 2 с, і записали 256 перехідних процесів, що призвело до загального часу збору 15,5 хв. Для обробки даних FID були аподизовані експоненціальним фільтром (розширення лінії (LB) 0,3 Гц), а плавник Уіттейкера застосовувався для автоматичної корекції базової лінії. Кількість точок було збільшено до 16 К у перетворених Фур'є спектрах. Сигнал TSP, встановлений на 0 ppm, використовувався як внутрішній еталон для вимірювання хімічного зсуву (δ).
3.4. Хімометрія
- Detoxi Slim Loss Швидке схуднення волокон Дієтичне схуднення Детокс Висока добавка
- FreeTrial Найкращий чай для схуднення в Інтернеті Найкращі таблетки для схуднення для чорношкірих вівчарських плацентарних дієт
- Китайські порошки для схуднення з дієтичного волокна для схуднення з молоком у Китаї - Китайські засоби для схуднення,
- Екстракт зеленого чаю для схуднення та схуднення Nature s Best
- Журавлино-мигдальні курячі котлети для схуднення - Світ для схуднення