Грип та ожиріння: його дивні стосунки та уроки пандемії COVID-19
Лівіо Лузі
1 Відділ ендокринології, харчування та метаболічних захворювань, IRCCS MultiMedica, Мілан, Італія
2 Відділ біомедичних наук та охорони здоров'я, Університет Міліана, Мілан, Італія
Марія Грація Радаеллі
1 Відділ ендокринології, харчування та захворювань метаболізму, IRCCS MultiMedica, Мілан, Італія
Анотація
Проаналізуйте взаємозв’язок ожиріння та грипу.
Методи
Базальне гормонове середовище, дефект реакції як вродженої, так і адаптивної імунної системи та малорухомість є основними факторами, що визначають ступінь тяжкості вірусної інфекції грипу у пацієнтів із ожирінням. Надмірна вага не тільки збільшує ризик інфікування та ускладнень для одинокої людини, що страждає ожирінням, але велика поширеність людей із ожирінням серед популяції може збільшити ймовірність появи більш вірулентного вірусного штаму, подовжує пролиття вірусу у всій популяції і, зрештою, може збільшити загальний рівень смертності від пандемії грипу.
Результати
Очікування на розробку вакцинації проти COVID-19, ізоляція позитивних випадків та соціальне дистанціювання є основними заходами. Тим не менше, дані попередніх пандемій грипу свідчать про такі втручання, спрямовані на поліпшення імунної відповіді: (1) схуднення з м’яким обмеженням калорій; (2) включати активатори AMPK та гамма-активатори PPAR до медикаментозного лікування ожиріння, асоційованого з діабетом; і (3) займатися фізичними вправами від помірних до помірних.
Висновки
Через тривале пролиття вірусів карантин у осіб із ожирінням, ймовірно, повинен бути довшим, ніж у осіб із нормальною вагою.
Вступ
Епідемія COVID-19 спричинена грипоподібним штамом вірусу (SARS-CoV-2). З часу «іспанської» пандемії грипу 1918 року відомо, що недоїдання (як недостатнє, так і надмірне) пов’язане з гіршим прогнозом вірусної інфекції [1]. "Азіатський" та "гонконгський" грипи 1957–1960 рр. Підтвердили, що ожиріння та діабет призводять до вищої смертності, а також до більш тривалої тривалості хвороби, навіть якщо суб’єкти не мали інших хронічних захворювань, що збільшують ризик грипу. пов'язані ускладнення [2, 3]. Під час пандемії H1N1 вірусу грипу А (IAV) 2009 року ожиріння також було пов’язане з підвищеним ризиком важких захворювань та фактором ризику для госпіталізації та смерті [4].
В індустріальних країнах близько 50% населення страждає від надмірної ваги або ожиріння, причому поширеність зростає щороку. В США останній звіт NHANES вказував, що 34% американців страждають ожирінням відповідно до критеріїв ВООЗ [5]. Одна модель Центру з контролю та профілактики захворювань (CDC) припускає, що від 160 до 210 мільйонів американців можуть заразитися цією хворобою протягом 12 місяців. На основі даних про смертність та поточних можливостей лікарні кількість смертей за сценаріями CDC коливалася від 200 000 до 1,7 мільйонів [6].
Тут ми представимо деякі міркування та докази щодо впливу високої поширеності ожиріння на дифузію та продовження епідемій COVID-19.
Чому пацієнти з ожирінням мають гіршу клінічну картину, ніж худі суб'єкти?
Ожирілі та страждають ожирінням діабетики змінюються на різних етапах вродженої та адаптивної імунної відповіді, що характеризується станом хронічного та слабкого запалення [7]. Цей шлях сприяє системній метаболічній дисфункції, яка пов’язана з розладами, пов’язаними з ожирінням.
По-перше, у пацієнтів із ожирінням хронічно вищі концентрації лептину (прозапальний адипокін) і нижчі концентрації адипонектину (протизапальний адипокін). Це несприятливе гормональне середовище також призводить до порушення регуляції імунної відповіді та може сприяти патогенезу ускладнень, пов’язаних із ожирінням [8]. У базальному стані пацієнти з ожирінням мають більш високу концентрацію кількох прозапальних цитокінів, таких як альфа-TNF, MCP-1 та IL-6, які в основному виробляються вісцеральною та підшкірною жировою тканиною, що призводить до дефекту вродженого імунітету [9]. Коли представлений антиген, хронічне запалення, пов’язане з ожирінням, спричиняє знижену активацію макрофагів та притуплену прозапальну продукцію цитокінів при стимуляції макрофагами [10]. Представлено знижену активацію макрофагів після антигену, що пояснює поганий успіх вакцинації пацієнтів із ожирінням [11]; це унікальне обезогенне мікросередовище пояснює появу антивірусно-стійких варіантів та варіантів уникнення вакцин у популяції ожиріння [11, 12]. Також реакції В і Т-клітин порушуються у пацієнтів із ожирінням та діабетом із ожирінням, і це спричиняє підвищену сприйнятливість та затримку вирішення вірусної інфекції.
Чжан та ін. припустив, що лептинова резистентність є фактором, що впливає на пандемічний грип 2009 року A (H1N1), причому лептин є основним регулятором дозрівання, розвитку та функції В-клітин [13]. Подібним чином, у пацієнтів із ожирінням можуть спостерігатися чисельні та функціональні зміни лімфоцитів, що призводять до погіршення реакції Т-клітин пам’яті та ефективності вакцини [14]. Ожиріння гальмує як специфічні для вірусу відповіді CD8 + Т-клітин, так і реакції антитіл на сезонну вакцину проти грипу; знову ж таки неоптимальна функціональність і зрілість макрофагів, що страждають ожирінням, може сприяти поганій реакції вакцини [15].
Дисрегульована протизапальна реакція сприяє важким ураженням легенів, що спостерігаються у постраждалих під час пандемії грипу. Потужна реакція CD8 + Т-клітин відіграє важливу роль у захисті від нових штамів та підтипів вірусу грипу.
Кілька досліджень щодо IAV-інфекції на мишах OB показують посилення тяжкості захворювання, збільшення вторинних бактеріальних інфекцій та зниження ефективності вакцини [16]. Насправді, у мишей із ожирінням спостерігається уповільнена та притуплена імунна відповідь, ймовірно, через знижений інтерферон (INF), адаптивні клітинні та опосередковані антитілами відповіді. Нещодавно Хонс та співавт. встановлено, що послідовне пасірування вірусу грипу H1N1 людини за допомогою моделей мишей, що страждають ожирінням (DIO) або мишей з генетичним ожирінням (OB), спричинених дієтою, призводить до більш вірулентного захворювання з підвищеною вірулентністю та захворюваністю; у моделі миші віруси глибокого секвенування виявили кілька мутацій вірусів, що переносяться хазяїном, і погіршення реакції інтерферону є дозвільним для генерації більш вірулентних популяцій IAV. Ці висновки не обмежені вірусним підтипом, а також виявлені в дослідженнях на людях. У нормальних клітинах бронхіального епітелію (NHBE), отриманих від осіб із ожирінням, було виявлено зменшену відповідь INF та посилену реплікацію вірусу грипу [16–18].
Іншою важливою проблемою серед осіб, що страждають ожирінням, є фізична бездіяльність. Малорухливість або знижена фізична активність характерні для пацієнтів із ожирінням щодо худих суб’єктів. Знижена фізична активність сама по собі [19] або опосередкована інсулінорезистентністю [20] погіршує імунну відповідь проти мікробних агентів на декількох етапах імунної відповіді, включаючи активацію макрофагів та інгібування прозапальних цитокінів.
Як фізична активність, так і фізичні вправи позитивно пов’язані із сприятливими результатами в метаболічному (діабет, ожиріння та метаболічний синдром) та імунологічному (рівні активації імунітету, ефективність вакцинації та старіння імунітету); втручання у фізичну активність продемонстрували потенціал зменшення ризику ускладнень шляхом модуляції запалення, посилення імунної системи та покращення результатів вакцинації у літніх людей [21].
Важливо також розглянути як потенційну причину гіршої клінічної картини людей із ожирінням динаміку легеневої вентиляції у цих суб'єктів із зменшеними діафрагмальними екскурсіями та відносним збільшенням простору анатомічної смерті.
Чому пацієнти з ожирінням потенційно заразніші, ніж худі суб’єкти?
Три фактори роблять людей, що страждають ожирінням, більш заразними, ніж худорляві: По-перше, люди з ожирінням, що страждають на грип, передають вірус протягом більш тривалого періоду часу (до 104% довше), ніж худі особини, що потенційно збільшує шанс розповсюдження вірусу на інших [22]. По-друге, ожиріне мікросередовище сприяє появі нових більш вірулентних штамів вірусів. Це пояснюється головним чином зниженою та уповільненою здатністю виробляти інтерферони ожиріними особинами та тваринами [17, 18]. Затримка у виробництві інтерферону проти контрастної реплікації вірусу дозволяє більше реплікації вірусної РНК, збільшуючи шанси появи нових, більш вірулентних вірусних штамів [18]. По-третє, індекс маси тіла позитивно корелює з інфекційним вірусом при видиху [23]. Ця знахідка була особливо значущою для чоловіків, що призводить до гіпотези, що більший об'єм вентиляції або диференціальна конформація грудної клітки можуть пояснити цей факт [23].
Чи може вірусна інфекція спричинити збільшення ваги?
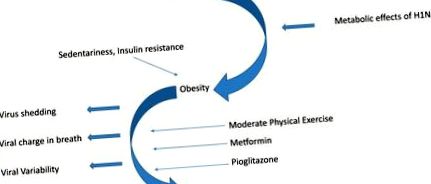
На рисунку схематизовано двонаправлений взаємозв'язок між грипом/грипоподібними вірусними інфекціями та ожирінням. Аденовірус 36 був пов'язаний з розвитком ожиріння. Стан ожиріння характеризується вищим зарядом вірусу при диханні та тривалим пролиттям вірусів. Втручання у спосіб життя та ліки, які зазвичай використовуються для лікування діабету, пов’язаного з ожирінням, викликають позитивну імунну модуляцію
Вплив вірусу грипу на інфіковані клітини ссавців, як правило, призводить до метаболічного зсуву у бік збільшення рівня гліколітиків та зменшення продукції АТФ [29]. Автори припускають, що початок апоптозу спричиняє цей метаболічний дисбаланс на пізній стадії процесу реплікації вірусу грипу [29]. Ця картина нагадує інсулінорезистентний стан із зниженням активності мітохондріального піруватдегідрогеназного комплексу (PDC), як правило, залученого до швидкості контролю окислення вуглеводів. PDC є важливим модулятором енергетичного та метаболічного гомеостазу, а резистентність до інсуліну пов’язана зі збільшенням піруватдегідрогеназикінази скелетних м’язів (PDK), яка фосфорилює та інактивує PDC. Підвищена експресія PDK4 у м’язах спостерігалася при інсулінорезистентному статусі, включаючи ожиріння [14, 30]. У мишей, інфікованих вірусом H1N1, спостерігається помітна регуляція активності PDC та рівня АТФ з вибірковою регуляцією PDK4 у скелетних м’язах, серці, печінці та легенях.
Для грипу характерні буря цитокінів та порушення обміну речовин. У цьому змаганні PDC відіграють важливу роль, каталізуючи окисне декарбоксилювання пірувату та пов'язуючи гліколіз із циклом трикарбонових кислот (ТСА) та синтезом жирних кислот. У мишей Yamane та співавт. [31] демонструють, що пероральне введення дихлорацетату (DADA, інгібітор PDK4) відновлює активність PDC та рівень АТФ, покращує порушення обміну речовин, пригнічує бурю цитокінів, регуляцію трипсину та реплікацію вірусу.
Які уроки можна взяти з попередніх інфекцій вірусу грипу при ожирінні?
Час інкубації COVID-19 вважається не більше 14 днів. Виходячи з концепції тривалого пролиття вірусу у людей із ожирінням [22], карантин слід подовжити у людей із ожирінням щодо худих суб’єктів, імовірно, удвічі. Поки конкретна вакцина недоступна, єдиними діями, які можна вжити, є ізоляція позитивних пацієнтів та посилення позитивної реакції імунної модуляції. Дієта та, головним чином, фізичні вправи як модулююча дія імунітету спрямована не тільки на схуднення, але й на швидке поліпшення імунної модуляції; захворюваність та смертність насправді можна зменшити регулярними фізичними вправами, навіть без значної втрати ваги. Кілька досліджень свідчать про те, що регулярні фізичні вправи підвищують рівень продукції цитокінів, опосередкований через TLR (сигнали, схожі на давальницькі рецептори) під час мікробної інфекції, покращуючи стійкість господаря до вторгнення патогенів [19]. Додатковою перевагою вправ є посилення системи антиоксидантного захисту та зменшення окисного стресу.
Уоррен та співавт. продемонструвати, що фізичні вправи покращують імунітет господаря до інфекції IAV як у мишей, що страждають ожирінням, так і у людей, що не страждають ожирінням. Зокрема, у мишей, що страждають ожирінням, фізична активність скасовувала пов’язані з ожирінням порушення імунного захисту господаря [32].
Результати свідчать про те, що фізична активність збільшувала імунну активацію (BAL-цитокіни, хемокіни та клітинна інфільтрація) на ранніх етапах зараження, «відновлюючи» імунну відповідь ожирених мишей до «нормального фенотипу»; насправді ожиріння затримувало імунну відповідь, а не повністю гальмувало її.
Вправи впливають на енергетичний баланс, а також на відповідь лептину, чутливість ІФН типу I, активацію PDC м’язів, крім того, збільшують сироваткові антигрипозні антитіла IgG2c і процентний вміст CD8 + Т-клітин у BAL; всі механізми можуть бути важливими для захисту господаря від інфекції [30, 32].
Таким чином, регулярні фізичні вправи виступають наріжним каменем як профілактичний захід для поліпшення захисту господаря проти вірусної інфекції грипу та інших метаболічних захворювань у осіб із ожирінням (але не тільки). Крім того, збільшення надмірної ваги та метаболічного синдрому серед підлітків у США [33, 34] та інших промислово розвинених країнах [35, 36] становить додаткову проблему. Насправді, будучи соціальним дистанціюванням єдиним профілактичним заходом, який можна вжити в очікуванні вакцини проти COVID-19, діти та підлітки становлять популяцію, де активізація соціальної дистанції є складнішою, ніж у дорослих, і де, мабуть, існує менше симптоматичне захворювання з більшим шансом мати безсимптомні носії вірусу.
Чи існує імуномодулююча терапія для профілактики грипу?
Найсильнішим, нефармакологічним, позитивним імуномодулюючим втручанням є фізичні вправи [37]. Помірні аеробні вправи (фітнес-ходьба, їзда на велосипеді, плавання, біг підтюпцем) мають протизапальну дію, зменшуючи альфа-TNF, MCP-1 та IL-6 та збільшуючи IL-10 [37]. Крім того, фізичні вправи спричиняють поліпшення середовища гормонів, збільшуючи чутливість до адипонектину та інсуліну та знижуючи рівень інсуліну та лептину, змінюючи змінене середовище гормонів у пацієнтів із ожирінням (рис. 1). На цьому шляху Zheng et al. показали, що регулярні фізичні вправи посилюють імунну відповідь проти мікробних антигенів у людини [19]. Цікаво відзначити, що позитивної імуномодуляції можна досягти лише за допомогою вправ м’якої та помірної інтенсивності. Навпаки, відомо, що інтенсивні або тривалі фізичні вправи (як біг марафону) виснажують імунну відповідь, головним чином, завдяки збільшенню ендогенного кортизолу [37]. Основним клітинним механізмом, за допомогою якого фізичні вправи надають більшу частину свого ефекту, є активація АМФ-кінази [38].
Окрім помірних фізичних вправ, було показано, що два класи препаратів, які зазвичай застосовуються у пацієнтів із ожирінням та/або діабетиком, позитивно модулюють імунну систему.
1. Активатори AMPK. Метформін (MET) є препаратом першої лінії для лікування цукрового діабету 2 типу і часто використовується не за призначенням для лікування декількох форм захворювань, пов’язаних з ожирінням (наприклад, СПКЯ). Метформін є потужним стимулятором активації AMPK, і, як ми довели, він зменшує осілість, збільшуючи активність у гризунів [38]. Це дослідження продемонструвало, що метформін покращує фізичну аеробну діяльність мишей, покращує утворення міотрубок та запобігає окисному стресовому пошкодженню, модулюючи сигналізацію ERK та SOD (супероксиддисмутази); тому ми висунули гіпотезу, що MET може також діяти як антиоксидант [37].
Інші опубліковані результати свідчать про те, що MET має прямий протизапальний ефект: Наприклад, MET знижує індуковану ліпополісахаридом протизапальну реакцію в моноцитах і макрофагах, знижує регуляцію клітин Th17, зменшує сигналізацію рецептора TNF-α та активацію NF-kB в ендотеліальному клітини і клітини гладких м’язів.
Diaz та співавт., In vivo та in vitro спостерігають зменшення внутрішнього запалення В-клітин та покращення реакції антитіл із подальшим збільшенням реакції на вакцину проти грипу у пацієнтів із діабетом 2 типу, які приймають MET. На закінчення, їх результати показують, що MET покращує реакцію В-клітин за рахунок зменшення внутрішнього запалення В-клітин та підвищення функції AMPK, тому AMPK може бути терапевтичною мішенню [39].
2. Більш конкретні активатори AMPK (AMP-активована протеїнкіназа), такі як AICAR (аміноімідазол карбоксамід рибонуклеотид), все ще вивчаються як модулятори імунітету. AMPK - це фермент, який надає протизапальну дію при активації, і він також визнаний стимулятором PPAR [40, 41]. У моделі миші Zhao et al. продемонстрував, що введення AICAR призводило до зменшення тяжкості ураження легенів та прозапальних процесів, що визначалося зменшенням накопичення нейтрофілів та зниженням рівня TNF-α та IL-6 у рідині бронхоальвеолярного промивання [42].
Мозлі та ін. повідомили про покращення виживання мишей, інфікованих вірусом грипу, які отримували AICAR, і про подальше покращення виживання (на 60%) за допомогою комбінованої терапії (AICAR + піоглітазон). Автори приходять до висновку, що результати їх дослідження дають попередні докази того, що стимулювання осі PPAR (агоністами AICAR та PPARγ) може виявитись сприятливим ефектом при важкій грипозній інфекції [41].
3. PPAR-гамма-активатори. Рецептори, що активуються проліфератором пероксисоми (PPAR), є ключовими регуляторами запалення та метаболізму ліпідів, їх активація призводить до зменшення запальних цитокінів (як IL6, INF γ) [40]. Розиглітазон та піоглітазон (два агоністи PPARγ) - це інсуліноміметичні препарати, що застосовуються при цукровому діабеті 2 типу з високим загальним потенціалом у зменшенні інфекції вірусу грипу [40]. Піоглітазон, здається, пригнічує запалення, зменшуючи експресію MCP-1, важливого медіатора запалення господаря [40]. Було показано, що піоглітазон збільшує виживання інфікованих мишей до 40%, і користь може бути пов’язана з модуляцією запальної реакції суб’єкта [40, 41]. Поєднання піоглітазону та AICAR збільшує виживання інфікованих мишей з 30 до 100% [41]. Тому агоністи метформіну, AICAR та PPARγ, як у комбінації, так і окремо, можуть бути вивчені, а потім використані при лікуванні важкого грипу разом із іншими противірусними/імуномодулюючими препаратами в майбутньому.
Висновки
Подяки
Ми вдячні пані К. Біасі за перегляд англійської мови. Ця робота була підтримана Міністерством охорони здоров'я Італії-Ricerca Corrente-IRCCS Multimedica.
- Психічне та фізичне здоров’я людей із ожирінням, постраждалих під час пандемії COVID-19 - UTHealth News -
- Як індустрія моди займається пандемією Covid-19
- Як спортивні бренди можуть допомогти в боротьбі з ожирінням у боротьбі з COVID-19 - Ганноверські комунікації
- Мексика націлена на шкідливу їжу, оскільки ожиріння набуває наслідків на тлі пандемії
- Високий кров'яний тиск, ожиріння та діабет, поширені у пацієнтів, госпіталізованих із COVID-19 NHLBI, NIH