Глутамат і ГАМК в регуляції апетиту
Тереза К. Дельгадо
1 Проміжна група метаболізму, Центр нейронаук та клітинної біології Коїмбри, Коїмбра, Португалія
Анотація
Регулювання апетиту: від периферії до гіпоталамуса
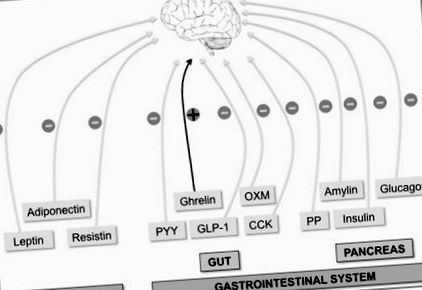
Мозок інтегрує безліч периферійних сигналів для контролю апетиту. Периферичні фактори, що свідчать про довготривалий енергетичний статус всього тіла, виробляються жировою тканиною (лептин, адипонектин та резистин). З іншого боку, гострий орексигенний (+) греліновий сигнал (виробляється в кишечнику) та анорексигенний (-) сигнали, такі як пептид кишкових гормонів YY (PYY), оксинтомодулін (OXM), глюкагоноподібний пептид-1 (GLP-1 ) та холецистокінін (CCK), а гормони підшлункової залози [інсулін, глюкагон, амілін та поліпептид підшлункової залози (PP)] вказують на тривалий енергетичний статус.
Дослідження, що використовують або дискретні ураження в гіпоталамусі (15, 16), або хірургічне пересічення (17) нервових шляхів, показали, що центральна інтеграція периферійних сигналів відбувається переважно в гіпоталамусі. Гіпоталамус лежить поруч з трьома окружними шлуночковими органами, які є зонами, що дозволяють речовинам залишати мозок, не порушуючи гематоенцефалічний бар'єр (ВГБ), тим самим дозволяючи іншим речовинам, які не перетинають ВВВ, здійснювати свої дії в мозку (18). . В останні роки було виявлено кілька нейромедіаторів, які беруть участь у регуляції апетиту гіпоталамусу [див., Наприклад, огляди (19–, 22)]. Наріжний експеримент з ідентифікації потенційного нейромедіатора полягає у введенні відповідного агента в гіпоталамус або сусідній шлуночок тваринних моделей та виявленні швидкого збільшення або зменшення споживання їжі. Ці експерименти дозволили не тільки ідентифікувати та охарактеризувати кілька нейромедіаторів, які беруть участь у регуляції апетиту гіпоталамуса, але й точно відстежувати шляхи, що містять ці сигнальні молекули. Зазвичай нейромедіатори класифікуються на пептиди, амінокислоти та моноаміни.
Гіпоталамічна пептидергічна нейротрансмісія та регулювання апетиту
У дугоподібному ядрі гіпоталамуса два набори нейрональних популяцій, що експресують або орексигенні нейропептиди [нейропептид Y (NPY) і пов'язаний з Агуті пептид (AgRP)], або анорексигенні нейропептиди [про-опіомеланокортин (POMC) і кокаїн-трансфектамін-амфетамін (КОРЗИНА)] співіснують. Нейропептид Y синтезується в нейронах, розташованих у далеко вентромедіальному аспекті дугоподібного ядра гіпоталамуса. У гіпоталамусі NPY-експресуючі волокна виступають з дугоподібного ядра в паравентрикулярне ядро, де виділяється пептид (23). Таким чином, введення NPY у паравентрикулярне ядро гіпоталамуса призводить до стійкого та стійкого збільшення споживання їжі у гризунів (24), що, зрештою, при повторному введенні призводить до ожиріння (25). З іншого боку, опосередкована антитілами блокада дії NPY призводить до зменшення споживання їжі у голодуючих тварин (26). Оскільки популяції нейронів, що експресують NPY, локалізовані спільно з нейронами, що вивільняють AgRP, оптогенетична (27) або фармако-генетична (28) стимуляція нейронів, що експресують AgRP, також стимулює інтенсивне споживання їжі, тоді як генетична абляція (29, 30) або фармако-генетична гальмування (28) зменшує споживання їжі.
Нейрони, розташовані головним чином у вентролатеральному підрозділі дугоподібного ядра гіпоталамуса, містять як анорексигенний пептид CART, так і його попередник POMC. Оптогенетична стимуляція нейронів, що містять POMC, зменшує споживання їжі (27), тоді як генетична абляція клітин, що експресують POMC (31, 32), збільшує апетит та споживання їжі. Ген, що кодує POMC, породжує пептидні продукти, що перебувають у потоці, включаючи меланокортини [адренокортикотропний гормон (АКТГ), α-, β- та γ-меланоцитостимулюючі гормони (MSH) та β-ендорфін (33). Вивільнення пептиду α-MSH у паравентрикулярному ядрі гіпоталамусу потенційно зменшує споживання їжі через активацію рецепторів меланокортину, MC3R та MC4R. Навпаки, збільшення споживання їжі та ожиріння сприймаються як результат делеції MC3R (34) та MC4R (35). Підводячи підсумок, активація РОМС-експресуючих нейронів у дугоподібному ядрі гіпоталамусу викликає вивільнення α-MSH, який активує MC4R у паравентрикулярному ядрі, що призводить до пригніченого споживання їжі та збільшення енергетичних витрат. З іншого боку, стимуляція AgRP-експресуючих нейронів у дугоподібному ядрі гіпоталамусу вивільняє пептид AgRP, який антагонізує дію α-MSH на MC4R, збільшуючи тим самим споживання їжі.
На сьогоднішній день найбільше зусиль було докладено до вивчення безпосередньої регуляції гіпоталамічних NPY/AgRP та POMC/CART-експресуючих нейронів різними циркулюючими факторами, тоді як ролі висхідних нервових входів приділено порівняно менше уваги. Це дивно, враховуючи, що як нейрони NPY/AgRP, так і POMC/CART отримують рясні збудливі та гальмівні синаптичні вхідні дані. Двома нейромедіаторами, на які припадає більша частина синаптичної активності в гіпоталамусі, є амінокислоти глутамат та γ-аміномасляна кислота (ГАМК).
Гіпоталамічний глутаматергічний нейромедіатор
Нейронно-астроцитарний метаболізм глутамату
Глутамат - це домінуючий збудливий нейромедіатор у центральній нервовій системі. Для того, щоб нейрон вивільняв глутамат, нейромедіатор повинен спочатку упаковуватися у високих концентраціях у синаптичні везикули за допомогою специфічних везикулярних транспортерів глутамату (VGLUT1, VGLUT2 та VGLUT3) (36). Після стимуляції глутамат вивільняється в синаптичну щілину, щоб зв’язати та викликати його вплив на постсинаптичні рецептори, будь то іонотропні [N-метил-d-аспартат (NMDA), d, l-альфа-аміно-3-гідрокси-5-метил- ізоксазол-пропіонова кислота (AMPA), каїнова кислота] або метаботропні рецептори (mGluRs), присутні як у нейронах, так і в астроцитах.
Глутамат в регуляції апетиту
Для оцінки ролі глутаматергічного введення до нейронів, що експресують NPY/AgRP та POMC/CART, і, більш конкретно, щодо його пластичності, регульованої глутаматними рецепторами NMDA, Liu et al. генерували мишей, у яких відсутні рецептори NMDA на нейронах AgRP або POMC (56). Автори виявили, що рецептори NMDA на нейронах AgRP, але не на нейронах, що експресують POMC, відіграють важливу роль у контролі енергетичного балансу, вказуючи на те, що активована натще активація нейронів, що вивільняють AgRP, пов'язана з помітно збільшеним вмістом глутаматергії (56). Крім того, завдяки поєднанню специфічних для клітин типу електрофізіологічних, фармакологічних та оптогенетичних методів, Ян та співавт. встановлено, що депривація їжі піднімає збудливий синаптичний вхід. Згідно з цими авторами, отриманий з кишечника грелін діє на пресинаптичні рецептори, щоб збільшити вивільнення глутамату та активувати нейрони, що експресують NPY/AgRP, за допомогою іонотропних рецепторів глутамату (57).
Гіпоталамічний ГАМК-ергічний нейромедіатор
Нейроно-астроцитарний ГАМК-ергічний метаболізм
ГАМК в регуляції апетиту
Стимулююча роль ГАМК у регуляції гіпоталамусової контрольованої поведінки годування була доведена протягом останніх років. Внутрішньоцеребровентрикулярне введення агоніста рецептора GABAA, мусцимолу, стимулює годування ситих свиней, блокуючи відповідь специфічним антагоністом рецептора GABAA, бікукуліном (68). Крім того, системне та внутрішньоцеребровентрикулярне введення агоніста рецептора GABAB, баклофену, спричинює збільшення споживання їжі у ситих свиней (69). Більше того, збільшене споживання їжі, отримане після введення баклофену, можна скасувати попередньою обробкою антагоністом рецептора ГАМК, факлофеном (69). На узгодження, кілька доказів вказують на те, що нейрони в дугоподібному ядрі гіпоталамуса експресують значною мірою транспортер GABA VGAT (70, 71), а також синтезуючі GABA ферменти GAD65 та GAD67 (70). За допомогою імуногістохімії було продемонстровано імунореактивність GAD65/GAD67 та GABA у більшості нейронів NPY/AgRP, розташованих у дугоподібному ядрі гіпоталамуса (70, 71). З іншого боку, не дивлячись на наявність мРНК GAD65/GAD67 приблизно у третини нейронів, що експресують POMC (72), VGAT не виявляли в тілах клітин POMC гіпоталамуса (53), що свідчить про відсутність вивільнення POMC GABA нейрони.
Вплив глутамату та ГАМК на механізм нейронально-астроцитарного метаболічного зчеплення, що лежить в основі регуляції гіпоталамічного апетиту
На сьогодні дії глутамату та ГАМК на механізм нейронально-астроцитарного метаболічного зв’язку, що лежить в основі регуляції апетиту гіпоталамусу, були в основному невивчені, головним чином, через відсутність відповідних методологічних підходів in vivo. Раніше було показано, що різноманітні методи магнітно-резонансної томографії (МРТ) та магнітно-резонансної спектроскопії (МРТ) надають вичерпну інформацію про мозкову активацію та основні механізми метаболічного зв’язку, що діють між нейронами та астроцитами. Однак порівняно великий розмір вокселів, використаний для отримання спектрів магнітно-резонансного резонансу in C vivo 13 виключає його використання для вивчення відносно зниженого апетиту, що контролює область гіпоталамусу дрібних гризунів. Крім того, спектроскопія ядерно-магнітного резонансу (ЯМР) високої роздільної здатності, що стосується мозкового метаболізму таких індикаторів, як [1–13 С] глюкоза або [2–13 С] ацетат, надала вичерпну інформацію про роботу нейронального та астроцитарного ТСА. цикли та міжклітинний обмін глутамат – глутаміном або ГАМК між нейронами та астроцитами цілого мозку [див., наприклад, (79–, 82)].
Тим не менше, порівняно велика кількість мозкової тканини, необхідна для підготовки екстрактів мозку для ЯМР-спектроскопії з високою роздільною здатністю 13 C, є важливим обмеженням. Щоб подолати вищезазначені обмеження, ЯМР-спектроскопія з магічним кутовим спінінгом з високою роздільною здатністю (HR-MAS) - техніка, що дає високоякісні спектри дуже дрібних біоптатів тканин (5–10 мг, розмір порівнянний з розміром гіпоталамусу мозку мишей. ) було запропоновано поліпшити просторову роздільну здатність та дослідити безпосередньо метаболізм гіпоталамусу. Тоді як 1 H HR-MAS ЯМР був використаний для метаболічного профілювання нормальних та хворих тканин (83), 13 C HR-MAS ЯМР-спектроскопія пропонує додаткову перевагу у наданні інформації про роботу метаболічних шляхів.
Заключні зауваження
Заява про конфлікт інтересів
Автори заявляють, що дослідження проводилось за відсутності будь-яких комерційних або фінансових відносин, які можна трактувати як потенційний конфлікт інтересів.
Подяка
TCD провів докторську стипендію від Fundação para a Ciência e Tecnologia, Португалія (SFRH/BPD/46197/2008).
- Дон; t Йди куди; s слизький - можливо, вам слід зіпсувати апетит
- Експериментальний препарат для схуднення знижує апетит, спалює більше енергії, дослідження передбачає FierceBiotech
- Китайський пригнічувач апетиту
- Пластирі для контролю апетиту Гуарана (60- або 90-графний) Groupon
- Таблетки для швидкого схуднення Ліда 💶 Потужний пригнічувач апетиту та спалювач жиру ✅ - CREA-RS