Дієтичний склад та фізіологічні пристосування до обмеження енергії
Анотація
Передумови
Концепція заданого значення маси тіла, що визначається переважно генетичними механізмами, була запропонована для пояснення поганих віддалених результатів звичайних дієт з обмеженим енергоспоживанням при лікуванні ожиріння.
Об’єктивна
Метою цього дослідження було вивчити, чи дієтичний склад впливає на гормональні та метаболічні пристосування до обмеження енергії.
Дизайн
Для порівняння ефектів дієти з обмеженим енергоспоживанням з високим глікемічним індексом та низьким глікемічним індексом (низький ГІ) був використаний рандомізований дизайн кросоверу. Склад макроелементів дієти з високим вмістом ГІ становив (у відсотках до енергії) 67% вуглеводів, 15% білків і 18% жиру, а в дієті з низьким вмістом ГІ 43% вуглеводів, 27% білків і 30% жирів; дієти мали однакову загальну енергію, щільність енергії та вміст клітковини. Випробовуваних, 10 юнаків із середньою вагою, вивчали протягом 9 днів двічі. У дні від -1 до 0 вони споживали самостійно підібрані продукти харчування за бажанням. 1–6 днів вони отримували дієту з високим або низьким вмістом шлунково-кишкового тракту з обмеженим енергоспоживанням. 7–8 днів дієти з високим або низьким рівнем шлунково-кишкового тракту вживались за бажанням.
Результати
Лептин у сироватці крові зменшувався меншою мірою з 0-го по 6-й день при дієті з високим вмістом шлунково-кишкового тракту, ніж при дієті з низьким рівнем шлунково-кишкового тракту. Витрати енергії у стані спокою зменшились на 10,5% під час дієти з високим вмістом шлунково-кишкового тракту, але лише на 4,6% під час дієти з низьким рівнем шлунково-кишкового тракту (7,38 ± 0,39 та 7,78 ± 0,36 МДж/день відповідно, у дні 5–6; P = 0,04). Баланс азоту, як правило, був більш негативним, а споживання енергії від закусок на 7-8 дні було більшим, при дієті з високим вмістом ГІ, ніж з низьким вмістом ГІ.
Висновок
Дієти з однаковим вмістом енергії можуть по-різному впливати на концентрацію лептину, витрати енергії, добровільне споживання їжі та баланс азоту, що припускає, що фізіологічні пристосування до обмеження енергії можуть бути змінені за допомогою дієтичного складу.
ВСТУП
Надмірна маса тіла є одним із найважливіших медичних станів у Сполучених Штатах, із поширеністю ≈25% у дітей (1) та> 50% у дорослих (2). Хоча наслідки для ожиріння для здоров'я та економічні витрати величезні (3), на сьогодні ефективного дієтичного лікування цієї проблеми не існує (4). Одне з пояснень поганих віддалених результатів звичайних дієт включає концепцію заданого значення маси тіла (5).
Результати численних досліджень свідчать про те, що вага тіла регулюється в межах певного діапазону. Коли худих або страждаючих ожирінням пацієнтів не годували, щоб досягти зміни маси тіла на 7,5–10%, загальні витрати енергії (ТЕЕ) зменшились на ≈12–15% (5–8). Інші фізіологічні зміни, викликані обмеженням енергії, включають посилення голоду та зниження регуляції нейроендокринних функцій (9–12). Ці адаптації разом можуть вплинути на подальшу втрату ваги. Відомо, що генетичні фактори впливають на діапазон регулювання маси тіла (13). Однак зростання поширеності ожиріння серед генетично стабільних популяцій (14) вказує на те, що навколишнє середовище також повинно відігравати важливу роль у регулюванні маси тіла.
ПРЕДМЕТИ І МЕТОДИ
Випробовувані були молоді чоловіки із середнім віком 27,9 років (діапазон: –18–34 роки), які мали помірно надмірну вагу [x ̄ ± індекс маси тіла (у кг/м 2): 30,6 ± 1,5, діапазон: 28,7–32,2) . В іншому обстежувані мали гарне самопочуття, як це визначали фізичний огляд та лабораторні дослідження (аналіз крові, глікозильований гемоглобін, функція щитовидної залози та функції печінки). Усі суб'єкти мали стабільну вагу (у межах 5% від поточної маси тіла протягом попередніх 6 місяців, шляхом самозвіту). Ми набирали сюжетів, рекламуючи через місцеві газети, листівки та радіо. Десять випробуваних успішно виконали протокол; один суб’єкт кинув дослідження, і його дані не були включені в результати. Дослідження було проведено в Загальному клінічному дослідницькому центрі (GCRC), Дитяча лікарня, Бостон, за схваленням Комітету з огляду установи та письмовій, інформованій згоді суб'єктів.
Експериментальний протокол слідував рандомізованій схемі кросоверу, що включала два 9-денних прийому до GCRC, розділених періодом змиву 2–6 тижнів. Протягом перших 2 днів кожного прийому (день -1 та день 0), суб'єкти споживали самостійно підібрану дієту за бажанням та отримували базові вимірювання. Протягом наступних 6 днів (дні 1–6) суб’єкти споживали або дієту з високим або низьким, і з низьким вмістом ГІ. У 7 та 8 дні випробовувані продовжували їсти дієти з високим або низьким вмістом шлунково-кишкового тракту, але їм дозволялося їсти додаткові страви за бажанням із приватного бару. Дослідження було завершено в обідній день на 8 день, що дозволило в цілому 34 години для споживання їжі ad libitum. Випробовувані повинні були робити щоденні вправи на біговій доріжці, поки не буде досягнуто 10% TEE. TEE визначали для кожного суб'єкта за рівнянням Гарріса-Бенедикта, помноженим на коефіцієнт активності 1,4 (28). До прийому до GCRC та між ними суб’єктам було доручено дотримуватися звичного режиму харчування та фізичних вправ, а також уникати кофеїну, алкоголю та тютюнових виробів.
Витрати енергії у спокої (РЗЕ) вимірювали за допомогою непрямої калориметрії натще (Vmax 29; SensorMedics Corporation, Yorba Linda, CA) загальною тривалістю 20–30 хв, поки випробовувані відпочивали в ліжку. Зразки крові отримували після вимірювання РЗЕ та перед сніданком. Крім того, зразки крові отримували 1-го дня кожні 30 хв за допомогою постійного венозного катетера для вимірювання реакцій глюкози та сироватки на інсулін у плазмі крові на сніданок, обід та вечерю для перевірки передбачуваних відмінностей у ШКТ (див. Нижче).
Таблиця 1
Одне з 2 змінних меню для дієт з високим глікемічним індексом (високий ГІ) та низьким глікемічним індексом (низький ГІ)
| Вуглеводи (% енергії) | 67 | 43 |
| Білок (% енергії) | 15 | 27 |
| Жир (% енергії) | 18 | 30 |
| Сніданок | Вівсяна каша (вівсяна каша швидкого приготування, 2% -жирне молоко з додаванням лактази, половинка вершків, декстроза, пшеничні висівки) Банан | Омлет (1 ціле яйце, 1 яєчний білок, шпинат, помідор, нежирний сир чеддер) Яблуко, з шкіркою Хліб з пумпернікелю Дієтичне желе |
| Обід | Сендвіч із запеченої яловичини (ростбіф, верхній круглий; пшеничний хліб; майонез; салат айсберг; помідор) Ізюм Курага Нежирний заморожений йогурт | Сендвіч з грудкою з індичкою (цільнозерновий 3-ядерний хліб, індичка без шкіри, майонез, салат айсберг) Салат (салат айсберг, селера, огірок, італійська заправка) Тушковані помідори Яблуко, з шкіркою Желатин без цукру |
| Вечеря | Куряча Джамбалая (довгозерний білий рис, варений; куряча грудка; масло; солодкий зелений солодкий перець; томатний соус; подрібнена цибуля) Кабачки з метеликів, варені Ангельський харчовий торт Знежирене молоко з доданою лактазою | Філе лосося Квасоля Солодкий червоний солодкий перець Вершкове масло Салат (салат айсберг, огірок, помідор, нежирна французька заправка) Хліб з пумпернікелю Грейпфрут |
| Перекус | Сендвіч з половиною індички (пшеничний хліб, копчена індича грудка, майонез, нежирний американський сир) Яблучний пюре, підсолоджений | Консервовані персики в легкому сиропі Сир з цільного молока Пів-пів вершків |
Зразки крові аналізували за допомогою таких інструментів або наборів: глюкоза в плазмі крові, аналізатор глюкози (APEC, Inc, Peabody, MA); сироватковий інсулін, Abbott IMx (Abbott Laboratories, Abbott Park, IL); та лептин із сироватки крові, набір для радіоімунологічного аналізу (Linco Research, Inc, St Charles, MO). Двадцять чотиригодинні збори сечі аналізували на вміст загального азоту за допомогою методу Кельдаля (29), а також аналізували на вміст креатиніну для оцінки адекватності збору. Баланс азоту, який повідомляється як середнє значення значень, отриманих на дні 3 і 6, обчислювали, використовуючи таке рівняння (30):
Площі під кривими глюкози та інсуліну визначали за допомогою правила трапеції (FIGP 2.98; програмне забезпечення BIOSOFT, Кембридж, Великобританія), а ефекти дієт порівнювали за допомогою парного критерію Стьюдента t. Зміни сироваткового лептину протягом двох дієт порівнювали за допомогою аналізу повторних вимірювань GLM (SPSS 9.0.0; SPSS Inc, Чикаго). Вплив дієти на РЗЕ наприкінці лікування (середнє значення днів 5 та 6) та зміна РЗЕ від вихідних значень оцінювали за допомогою парних t-тестів. Результати повідомляються як середні (± SEM).
РЕЗУЛЬТАТИ
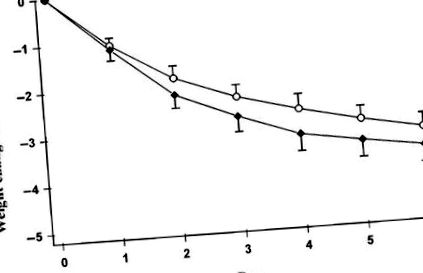
Втрата ваги суттєво не відрізнялася між двома дієтами (3,62 ± 1,14 кг при дієті з низьким вмістом ГІ та 3,23 ± 0,92 кг при дієті з високим вмістом ГІ), як показано на малюнку 1. Середня площа під кривою глікемічної відповіді була вдвічі більшою при дієті з високим вмістом шлунково-кишкового тракту (2,69 ± 0,47 ммоль · год/л), ніж при дієті з низьким рівнем шлунково-кишкового тракту (1,30 ± 0,19 ммоль · год/л; Р = 0,001). Середня площа під кривою інсулінемічної відповіді була майже на 50% більшою при дієті з високим вмістом шлунково-кишкового тракту (700 ± 98,4 пмоль · год/л), ніж при дієті з низьким рівнем шлунково-кишкового тракту (478 ± 82,2 пмоль · год/л; Р = 0,01) (Малюнок 2).
Середня (± SEM) втрата ваги від базової лінії протягом 6 днів обмеження енергії. Базова маса для дієти з високим глікемічним індексом (○) становила 98,5 ± 2,7 кг, а для дієти з низьким глікемічним індексом (◆) - 99,2 ± 2,9 кг (НС; n = 10).
Глікемічна (А) та інсулінемічна (В) відповіді, виміряні з інтервалом у 0,5 години. Криві є середніми значеннями (± SEM) після сніданку, обіду та вечері 1-го дня. Колонки представляють площу під кривою концентрації та часу, розрахованої з використанням правила трапеції. Фактичний вихідний рівень глюкози в крові для дієти з високим глікемічним індексом (high) становив 5,5 ± 0,2 ммоль/л, а для дієти з низьким глікемічним індексом (low) - 5,3 ± 0,2 ммоль/L (NS; n = 10).
Лептин у сироватці крові (рисунок 3) знижувався швидше і більшою мірою під час дієти з низьким вмістом шлунково-кишкового тракту, ніж під час дієти з високим рівнем шлунково-кишкового тракту (Р = 0,03). До 6-го дня лептин знизився на 50,0 ± 5,5% від вихідного рівня при дієті з низьким вмістом шлунково-кишкового тракту, порівняно з 38,3 ± 3,5% при дієті з високим рівнем шлунково-кишкового тракту.
Середнє значення (± SEM) добового сироваткового лептину натще як відсоток від базових значень. Базовий сироватковий лептин для дієти з високим глікемічним індексом (○) становив 14,9 ± 1,7 мг/л, а для дієти з низьким глікемічним індексом - 13,4 ± 1,2 мг/л (NS; n = 10).
РЗЕ (малюнок 4) зменшився від вихідного рівня до кінця періоду обмеження енергії (середнє значення днів 5 і 6) на 4,6% при дієті з низьким рівнем ГІ (Р = 0,03) та на 10,5% при дієті з високим ГІ ( Р = 0,005). Середня РЗЕ була нижчою на 5 і 6 день дієти з високим рівнем шлунково-кишкового тракту (7,38 ± 0,39 МДж/добу), ніж на 5 і 6 день дієти з низьким рівнем шлунково-кишкового тракту (7,78 ± 0,36 МДж/добу; Р = 0,04).
Середні (± SEM) щоденні витрати енергії в стані спокою при дієтах з високим (○) та низьким (◆) глікемічним індексом (n = 10).
Баланс азоту був позитивним при дієті з низьким вмістом шлунково-кишкового тракту і негативним при дієті з високим рівнем шлунково-кишкового тракту (25,7 ± 14,1 та −9,7 ± 5,5 мг N · кг −1 · d −1 відповідно; P = 0,06).
Споживання їжі в режимі ad libitum протягом 7 та 8 днів було на 25% більшим при дієті з високим вмістом шлунково-кишкового тракту (17,0 ± 2,2 МДж), ніж при дієті з низьким рівнем шлунково-кишкового тракту (13,5 ± 1,9 МДж; Р = 0,009). Оцінки смакових якостей їжі ad libitum суттєво не відрізнялись між дієтами (7,2 ± 0,8 при дієті з високим рівнем шлунково-кишкового тракту і 6,3 ± 0,9 при дієті з низьким рівнем шлунково-кишкового тракту).
ОБГОВОРЕННЯ
Звичайні дієти з обмеженим енергоспоживанням мають дуже погані довгострокові результати щодо втрати ваги (4), можливо тому, що ці дієти викликають зміни голоду та обміну речовин, що сприяють відновленню ваги (5). Результати цього дослідження показують, що дієтичний склад може змінювати фізіологічні пристосування до обмеження енергії, що може мати значення для розробки нових дієтичних методів лікування ожиріння.
Втрата ваги суттєво не відрізнялася між дієтою з високим та низьким вмістом шлунку, як і слід було очікувати від однакової енергетичної дієти. Однак сироватковий лептин зменшився більшою мірою при дієті з низьким рівнем шлунково-кишкового тракту. Цю різницю можна пояснити нижчими концентраціями інсуліну, пов'язаними з цією дієтою, оскільки інсулін є лептиновим секретагогом (31, 32), або зниженням метаболізму глюкози в адипоцитах (33). Це спостереження узгоджується з результатами Jenkins та співавт. (34), які показали позитивну зв'язок між споживанням вуглеводів та концентрацією лептину під час обмеження енергії. Цікаво, що нижча концентрація лептину при дієті з низьким вмістом шлунково-кишкового тракту спостерігалася без ознак підвищеного голоду (споживання їжі ad libitum насправді було нижчим при цій дієті), що свідчить про функціональне покращення стійкості до лептину, пов’язане з ожирінням (35, 36). Потрібно подальше розслідування значення цього явища.
РЗЕ зменшився меншою мірою при низькому вмісті ГІ, ніж при дієті з високим вмістом ГІ. Відповідно до цього висновку Уайтхед та співавт. (37) показали, що швидкість метаболізму уві сні знижується менш швидко при високобілковій дієті, ніж при низькобілковій дієті. У цьому дослідженні дієта з низьким вмістом ГІ містила більше білка, ніж дієта з високим вмістом ГІ. Однак ми зазначаємо, що нинішні результати не були спричинені підвищеним термічним ефектом білка порівняно з ефектом інших макроелементів, оскільки швидкість метаболізму вимірювали через 10 годин після останнього прийому їжі. Збереження РЗЕ під час обмеження енергії за допомогою дієти з низьким вмістом ГІ, разом із різницею у добровільному споживанні їжі та ситості, показаною нами та іншими (21–26), свідчить про те, що дієти з низьким вмістом ГІ можуть переноситися краще, ніж дієти з високим вмістом ГІ.
Підводячи підсумок, це дослідження продемонструвало сприятливі ефекти дієти з низьким вмістом жиру із середнім вмістом жиру порівняно з дієтою з високим вмістом жиру та з низьким вмістом жиру, що відповідає сучасним рекомендаціям щодо харчування. Цей висновок свідчить про те, що гормональні та метаболічні реакції на обмеження енергії - включаючи концентрації лептину, витрати енергії, добровільне вживання їжі та азотний баланс - можуть впливати на дієтичний склад. Потрібні додаткові дослідження, щоб підтвердити ці результати в інших популяціях та протягом більш тривалого періоду, визначити, які конкретні дієтичні фактори опосередковують ці фізіологічні події, та вивчити довгостроковий вплив ШКТ на регуляцію маси тіла.
Подяка
Ми дякуємо медперсоналу GCRC у Дитячій лікарні, Бостон; персонал метаболічної кухні в Бригамі та жіночій лікарні, Бостон; та Кейт Донован, без якої дослідження не було б можливим.
За підтримки грантів Фонду Чарльза Гуда, Фонду ендокринних стипендіатів, фармацевтичної компанії Knoll, Загального клінічного дослідницького центру (M01 RR02172, M01 RR02635) та Національного інституту діабету та захворювань органів травлення та нирок (до DSL; 1K08 DK02440).
- Щільність дієтичної енергії позитивно пов’язана з ризиком раку підшлункової залози в міському Шанхаї
- Дієтичні харчові звички та контрольоване тренування складу тіла та сили у елітних жінок
- Дієтичні втручання для обмеження росту плода - терапевтичний потенціал дієтичної нітрату
- Дієтичні емульгатори безпосередньо змінюють склад мікробіоти людини та експресію генів ex vivo
- Дієтичні співвідношення жиру та ліпідний склад плазматичної мембрани печінки SpringerLink