Безпека та ефективність глюкоманнану для зниження ваги у дорослих із надмірною вагою та середнім ожирінням
1 Коледж медсестер Університету Раша, 600 S. Paulina Street, Suite 1080, Chicago, IL 60612, USA
2 Медичний центр Університету Раша, 1725 W. Harrison Street, Чикаго, Іллінойс, 60612, США
3 Секція гастроентерології та харчування, Медичний центр Університету Раша, 1725 W. Harrison Street, Чикаго, Іллінойс, 60612, США
4 Школа медсестер університету Північного парку, 3225 W. Foster Avenue, Чикаго, штат Іллінойс, 60625, США
5 Спільнота, системи та догляд за психічним здоров’ям, Університетський коледж Раша, 600 S. Paulina Street, Suite 1080, Chicago, IL 60612, USA
6 Факультетська практика, Коледж медсестер Університету Раша, 600 S. Paulina Street, Suite 1080, Chicago, IL 60612, USA
Анотація
Передумови. Небагато безпечних та ефективних дієтичних добавок, що сприяють зниженню ваги. Ми оцінили безпеку та ефективність глюкоманнану, водорозчинної добавки клітковини, для досягнення втрати ваги у осіб із надмірною вагою та середнім ожирінням, які споживають самостійно підібрані дієти. Методи. Учасникам було випадково призначено приймати 1,33 грама глюкоманнану або капсули плацебо з однаковим виглядом з 236,6 мл води за годину до сніданку, обіду та вечері протягом 8 тижнів. Первинним результатом ефективності була зміна маси тіла через 8 тижнів. Іншими результатами ефективності були зміни в складі тіла, голоді/повноті та концентрації ліпідів та глюкози. Результати безпеки включали шлунково-кишкові симптоми/толерантність та рівень печінкових ферментів у сироватці крові та рівень креатиніну. Результати. Всього було включено та рандомізовано 53 учасників (віком 18–65 років; ІМТ 25–35 кг/м 2). Ці дві групи не відрізнялись щодо базових характеристик та відповідності доповненню до дослідження. Через 8 тижнів не було суттєвої різниці між групами глюкоманнану та плацебо у кількості втрати ваги (
, відповідно) або інших результатів ефективності або будь-яких результатів безпеки. Висновки. Добавки глюкоманнану, які вводили протягом 8 тижнів, добре переносились, але не сприяли зниженню ваги або суттєво не змінювали склад тіла, голод/повноту або параметри ліпідів та глюкози. Ця пробна версія зареєстрована на NCT00613600.
1. Вступ
Надмірну вагу та ожиріння надзвичайно важко повернути назад. Незважаючи на широке використання традиційних стратегій управління - низькокалорійних дієт, фізичної активності, поведінкових втручань та фармакологічних препаратів - поширеність надмірної ваги та ожиріння продовжує зростати в США. За оцінками, 65% усіх дорослих людей США мали надлишкову вагу або страждали ожирінням протягом 2007-2008 років [1]. Надмірна вага та ожиріння збільшують ризик супутніх захворювань, таких як діабет та атеросклероз, і пов’язані зі зниженням якості життя та тривалості життя [2, 3]. Очевидно, що потрібні альтернативні підходи. Одним з потенційно перспективних альтернативних підходів є глюкоманнан - дієтична добавка, яка широко рекламується та використовується для зниження ваги. Незважаючи на широке використання, безпека та ефективність глюкоманнану недостатньо вивчені.
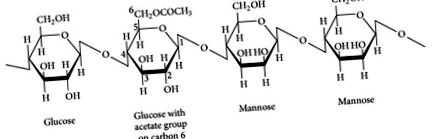
Глюкоманнан - це водорозчинна, ферментована харчова клітковина, витягнута з бульби або кореня слонового ямса, також відомого як коньяк (Amorphophallus konjac або Amorphophallus rivieri). Глюкоманнан складається з полісахаридного ланцюга бета-D-глюкози та бета-D-маннози з приєднаними ацетильними групами у молярному співвідношенні 1: 1,6 із зв'язками бета-1-4 (див. Малюнок 1) [4-6]. Оскільки слина людини і амілаза підшлункової залози не можуть розщеплювати зв’язки бета-1, 4, глюкоманнан відносно незмінно переходить у товсту кишку, де вона сильно ферментується бактеріями товстої кишки. Він має високу молекулярну масу (в середньому: 1 000 000 Дальтон) і може поглинати у воді до 50 разів більше своєї ваги, що робить його одним з найбільш в’язких харчових волокон, відомих [6]. Отже, глюкоманнан приймають у менших дозах, ніж інші типи волоконних добавок.
Вважається, що механізми, що опосередковують ефекти зниження ваги глюкоманнану, подібні до механізмів інших розчинних у воді ферментованих волокон. Зі своєю низькою щільністю енергії та об’ємними властивостями, глюкоманнан, здається, сприяє зниженню ваги, витісняючи енергію інших поживних речовин та виробляючи ситість та ситість, поглинаючи воду та розширюючись у шлунково-кишковому тракті. Крім того, глюкоманнан, здається, знижує рівень загального холестерину та ліпопротеїдів низької щільності (ЛПНЩ), стимулюючи фекальну екскрецію холестерину та жовчних кислот та зменшуючи всмоктування холестерину в кишечнику [7–9]. Крім того, глюкоманнан може покращувати глікемічні параметри, гальмуючи апетит та уповільнюючи кишкове всмоктування через підвищену в'язкість [10–13]. Як правило, глюкоманнан добре переноситься і має сприятливий профіль безпеки.
Глюкоманнан був пов’язаний зі зниженням маси тіла та рівня ліпідів та глюкози у плазмі крові у дорослих у кількох клінічних випробуваннях [14–19]. Але ці випробування були обмежені слабким дизайном, малими розмірами зразків, неоднорідними діагнозами, варіативними рецептурами та дозуванням глюкоманнану та короткою тривалістю спостереження [20]. На відміну від цих досліджень, ми використовували рандомізовану, подвійну сліпу, плацебо-контрольовану конструкцію для оцінки безпеки та ефективності 3,99 г/день капсул глюкоманнану у зразку 53 здорових людей із надмірною вагою та середнім ожирінням, які споживали самостійно підібрані дієти та підтримання звичного рівня фізичної активності протягом 8-тижневого періоду навчання.
2. Матеріали та методи
2.1. Дослідження населення
На основі попереднього плацебо-контрольованого дослідження глюкоманнану [18], ми планували набрати 50 учасників і спостерігати за ними протягом 8 тижнів, щоб мати 80% потужності для адекватного виявлення змін у вазі та інших метаболічних змінних.
2.2. Вивчати дизайн
Особам, які відповідали вимогам та дали згоду на участь у дослідженні, було довільно призначено отримувати капсули, що містять глюкоманнан або відповідне плацебо, наповнене неактивною мікрокристалічною целюлозою. Для створення послідовності рандомізації використовувався генератор випадкових чисел; коробки, що містять запас капсул кожного учасника, були упаковані відповідно до цієї послідовності. І капсули глюкоманнану, і плацебо були приготовані зовнішньою аптекою, яка не мала іншої ролі у дослідженні. Щоб переконатися, що добавка глюкоманнану, що використовувалась протягом досліджуваного періоду, відповідала стандартам контролю якості, її купували з тієї ж партії, а зразок подавали на ConsumerLab.com для аналізу складу та чистоти, де вказували відповідний склад та чистоту. Ні учасники, ні слідчі не знали про призначення лікування.
Учасникам було наказано приймати дві капсули глюкоманнану або 1,36 г (1,33 г) глюкоманнану з 236,6 мл води за годину до сніданку, обіду та вечері протягом 8 тижнів (загалом 3,99 г/день). Їм також пропонувалося підтримувати поточний рівень споживання їжі та рівень фізичної активності. Учасники дослідження повернулися через 2 тижні та 8 тижнів, щоб повернути будь-яке невикористане доповнення до дослідження або плацебо з попереднього візиту, отримати новий запас доповнення до дослідження або плацебо протягом решти 6 тижнів, повідомити про побічні ефекти та взяти кров.
Усі дані були зібрані дослідницьким персоналом та завантажені в базу даних TeleForm (електронне сканування) асистентом. Дослідження було схвалено комісією з огляду сайту. Усі учасники надали письмову інформовану згоду перед зарахуванням. Незалежна комісія з моніторингу даних та безпеки моніторила випробування та переглядала проміжні результати.
2.3. Первинний результат
Первинним результатом ефективності стала втрата ваги від початкового рівня до 2 тижнів та 8 тижнів після рандомізації. Вагу тіла вимірювали з точністю до 1/10 кг за допомогою відкаліброваної електронної ваги, при цьому учасники носили легкий одяг без взуття [21].
2.4. Вторинні результати
Вторинні результати ефективності включали зміни у складі тіла (окружність талії/стегон, жир і маса без жиру), голод та повнота, а також показники ліпідів та глюкози в крові натще. Окружність талії та стегон визначали за допомогою стандартизованих процедур [22], а жир і знежирену масу тіла вимірювали за допомогою шкали Tanita Ultimate Scale (Tanita Corp., Токіо, Японія). Суб'єктивні відчуття голоду та ситості оцінювали за допомогою стандартизованих 100-міліметрових візуальних аналогових ваг (VAS) [23]. Шкала голоду була закріплена словами: "Зовсім не голодний" і "Надзвичайно голодний", а шкала повноти - "Зовсім не повний" і "Надзвичайно ситий". Учасникам було запропоновано зробити вертикальну відмітку через лінію, що відповідає їх почуттям протягом останніх чотирьох годин у день їх запланованого візиту в клініку (всього = три дні протягом 8-тижневого періоду дослідження). Для оцінки шкал відстань у мм від 0 для кожної шкали вимірювали лінійкою. Зразки периферичної венозної крові натощак отримували на рівні глюкози та ліпідів. Для кількісної оцінки тригліцеридів, загального холестерину та холестерину ЛПВЩ використовували стандартну ліпідну панель; Рівні холестерину ЛПНЩ розраховували за допомогою рівняння Фрідевальда.
Ключовими результатами безпеки були шлунково-кишкові симптоми та переносимість та лабораторна оцінка функції печінки та нирок. Шлунково-кишкові симптоми та толерантність визначали, запитуючи учасників про труднощі з ковтанням, здуття живота, діарею, відрижку та інші симптоми, пов’язані з шлунково-кишковим трактом, за допомогою стандартних методів непрямого опитування, включаючи початок симптомів та чи вважалося, що вони пов’язані з додатком до дослідження. Ферменти печінки вважалися підвищеними при рівні аспартатамінотрансферази> 275 од/л та/або аланін-трансферазі> 250 од/л; для креатиніну в сироватці крові рівень> 4,5 мг/дл вважався підвищеним.
Інші заходи включали споживання дієти, фізичну активність, дотримання добавок та сприйняття довіри/очікуваності досліджуваного лікування. Щоб оцінити зміни протягом 8-тижневого періоду дослідження, споживання дієти вимірювали за допомогою 3-денних записів про їжу, заповнених на початковому рівні, 2 тижні та 8 тижнів, та аналізували за допомогою програмного забезпечення для аналізу клінічних даних NutriBase (http://www.nutribase.com /). Міжнародну анкету з фізичної активності (IPAQ) [24] вводили на початковому етапі, 2 тижні та 8 тижнів, щоб охарактеризувати будь-які зміни у звичайному рівні активності протягом періоду дослідження, які можуть вплинути на результати дослідження. Відповідність добавкам вимірювали за кількістю капсул та самостійним звітом про відсоток прийнятих капсул. Розрахункова відповідність визначалася як відсоток призначених доз, взятих від вихідного рівня протягом 8-тижневого періоду дослідження. Оскільки розбіжності у сприйнятті учасниками довіри до обґрунтування лікування та їх тривалості можуть заплутати висновки, ми запросили Анкету довіри/очікуваності (CEQ) для учасників обох груп у перший та останній дні лікування [25].
2.5. Статистичний аналіз
Всі статистичні аналізи проводили за допомогою SPSS 16.0 (Чикаго, Іллінойс). Для характеристики вибірки використовували описову статистику. Номінальні дані аналізували за допомогою критерію хі-квадрат, тоді як безперервні дані аналізували за допомогою кореляційного аналізу Пірсона, незалежної вибірки
-тести та односторонній дисперсійний аналіз. Дані представлені як середнє значення ± SD. Визначено рівень значущості 0,05 апріорі.
3. Результати
3.1. Дослідження населення
На малюнку 2 зображено скринінг, зарахування та подальші спостереження за учасниками випробування. З 124 перевірених дорослих загалом 53 відповідали критеріям прийнятності та були включені в дослідження. Двадцять шість учасників були випадковим чином віднесені до групи глюкоманнану, а двадцять сім учасників до групи плацебо. Суттєвих відмінностей між двома групами у швидкості припинення лікування не було. По три учасники в кожній групі були або втрачені для подальшого спостереження, або припинили дослідження з особистих причин, що призвело до остаточної вибірки з 47 учасників.
Базові демографічні та клінічні характеристики були однаковими між двома групами (табл. 1). Учасники були переважно жінки (
85%), представляли поєднання расових та етнічних груп та мали середній вік 40,6 років. Для 47 учасників, які завершили дослідження, розрахована відповідність становила 81,3% ± 4,5% у групі глюкоманнану та 82,7% ± 5% у групі плацебо.
- Знання в галузі харчування пов’язані з більшою втратою ваги у людей із ожирінням та надмірною вагою із низьким рівнем доходу
- Фізіологічні зусилля в субмаксимальних фітнес-тестах передбачають втрату ваги у чоловіків із надмірною вагою та ожирінням
- Безпека та ефективність ледіпасвіру Софосбувір у дорослих із хронічною інфекцією ВГС - Повний текст
- Бордер-коллі, що страждає ожирінням, починає подорож до схуднення, говорить собака-рятувальник Вінніпег - Вінніпег
- Дослідження тренера з охорони здоров'я AI покращує втрату ваги серед людей із ожирінням